阿尔兹海默疾病模型
一、勋博生物AD动物模型的分类与构建原理
根据病理模拟机制,AD动物模型主要分为三大类:
转基因模型:通过基因编辑技术导入人类AD相关突变基因,模拟遗传性AD的病理进程。常见模型:
-
- APP单转基因模型(如Tg2576、PDAPP小鼠):将人类APP基因(含瑞典突变K670N/M671L等)导入小鼠基因组,促进Aβ过度产生。通过原核显微注射技术将外源基因片段(含启动子、APP cDNA、PolyA尾)注入受精卵,筛选阳性后代。
- 双/多转基因模型(如APP/PS1、3xTg-AD、5xFAD小鼠):
- APP/PS1:共表达APP(Swedish突变)和PSEN1(M146L突变)基因,加速Aβ沉积。
- 3xTg-AD:同时携带APP(Swedish)、PS1(M146V)和Tau(P301L)突变,兼具Aβ斑块与神经纤维缠结(NFTs)。
- 5xFAD:整合5个家族性AD突变(APP K670N/M671L + I716V + V717I;PSEN1 M146L + L286V),在2-3月龄即出现Aβ沉积和神经元死亡。
非转基因诱导模型:通过物理、化学或手术干预诱导AD样病理改变。
-
- 化学诱导模型:
- Aβ注射模型:向大鼠/小鼠双侧海马或侧脑室注射聚集态Aβ片段(Aβ1-40、Aβ1-42或Aβ25-35),浓度通常为1-5 μg/μL,注射量2-5 μL/侧。
- 材料:立体定位仪、微量注射泵、Aβ冻干粉(需预聚集处理)。
- 胆碱能损伤模型:
- 东莨菪碱(SCOP) :腹腔注射(0.2 mL/150g,连续14天),阻断胆碱能受体。
- 鹅蒿蕈氨酸(IBO) :脑内注射(5-10 μg/μL)破坏基底前脑胆碱能神经元。
- 金属离子诱导:
三氯化铝(AlCl3) :腹腔注射(100 mg/kg,60天)或脑室内注射(2.5%,3μL),促进Tau磷酸化。
- 代谢损伤模型: 皮下注射(D-半乳糖(D-gal)50-150 mg/kg,6-8周)联合铝盐,加速氧化应激和神经元凋亡。
- 化学诱导模型:
物理损伤模型:
-
-
- 海马伞横断术:
- 手术:手术切断海马伞通路,导致胆碱能神经元退行性变。
- 操作:颅骨钻孔后,用弯曲针头插入海马坐标(前囟后2.4mm,矢状缝旁2.0mm,深度3mm),旋转破坏组织。
- 颈动脉结扎:单/双侧颈总动脉永久结扎,或结合颈动脉狭窄术,诱导脑缺血和认知障碍。
- 海马伞横断术:
-
衰老模型:模拟自然衰老过程中的AD病理。
-
- 自然衰老模型:使用老年灵长类(猕猴)或啮齿类(24月龄以上大鼠),需长期饲养(>18个月)。
- 加速衰老模型:快速老化小鼠(SAM) :源于AKR系小鼠,6月龄自发出现Aβ沉积和认知障碍。D-半乳糖联合诱导:皮下注射D-gal(100 mg/kg)联合AlCl₃(200 mg/kg),缩短造模时间至8周。
二、勋博生物AD模型常用实验动物及选择依据
| 动物种类 | 优势 | 局限性 | 适用模型类型 |
|---|---|---|---|
| 小鼠
(C57BL/6, FVB) |
繁殖快、成本低、基因编辑成熟;学习能力较强 | 脑体积小,NFTs形成不典型 | 转基因、化学诱导 |
| 大鼠
(Wistar, SD) |
脑结构更接近人类,手术操作便利 | 自然AD病理较少 | 手术损伤、化学诱导 |
| 非人灵长类
(恒河猴) |
脑结构与人类高度相似,自发Aβ沉积和NFTs | 成本高、伦理限制、繁殖周期长 | 自然衰老、转基因 |
| 新型模型
(斑马鱼、果蝇) |
适用于高通量筛选和早期机制研究 | 神经系统简化,缺乏高级认知 | 基因突变快速筛选 |
三、勋博生物AD模型有效性评估指标
病理学特征检测
-
- Aβ沉积:硫黄素S染色或Aβ免疫组化(如6E10抗体)。
- Tau蛋白磷酸化:Western Blot检测p-Tau(Thr231/Ser396位点)。
- 神经元丢失:尼氏染色或NeuN免疫组化。
行为学测试(核心认知功能评估)
| 测试名称 | 检测功能 | 操作要点 |
|---|---|---|
| Morris水迷宫 | 空间学习记忆 | 记录动物找到隐藏平台的时间(潜伏期) |
| 新物体识别 | 短期记忆 | 比较动物探索新/旧物体的时间比 |
| 场景恐惧实验 | 情境记忆 | 测定僵直时间反映关联恐惧记忆 |
| 放射臂迷宫 | 工作记忆 | 记录重复进入无食物臂的错误次数 |
生化指标
-
- Aβ40/Aβ42比值:ELISA检测脑匀浆,比值升高预示病理加重。
- 炎症因子:IL-1β、TNF-α水平(ELISA或qPCR)。
- 胆碱能标志物:乙酰胆碱酯酶(AChE)活性测定。
四、勋博生物AD模型典型案例介绍:
- 双侧海马立体定向注射Aβ1-42诱导阿尔茨海默症小鼠模型:
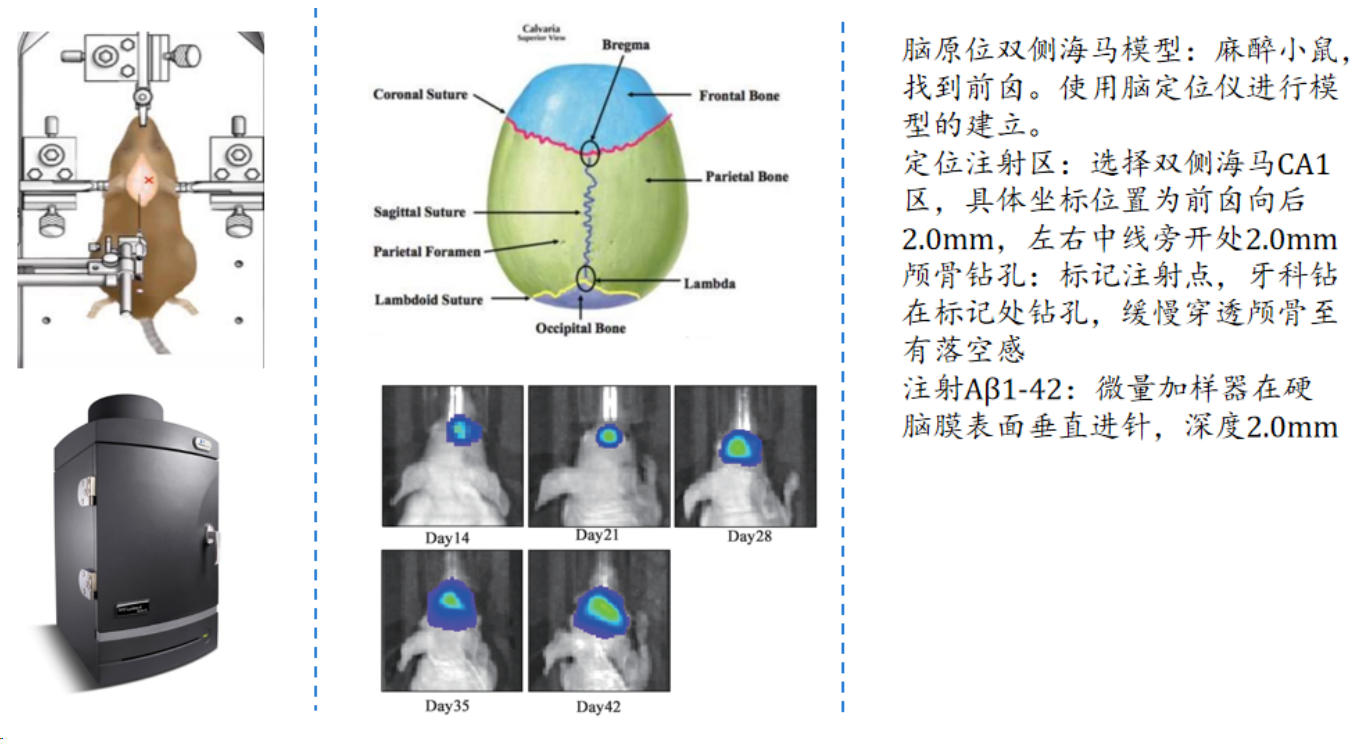
Morris水迷宫验证模型:
Morris 水迷宫中黑色水池直径3750px,高1500px。隐形平台(10×10×700px)或圆形透明平台。
圆桶中注水高度1125px,平台位于水面下25px。水温维持在20-22°C,水中加入染料混匀使平台隐蔽。实验分为三个阶段。
-
-
- 适应期:实验开始前1天每只小鼠置于水迷宫实验室以适应周围环境;
- 训练期:在前5天的定位航行实验中,每天测试4次,均从不同的象限入水。每轮实验将小鼠从设定的入水点面向池壁放入水中。如果60s内实验小鼠爬上隐蔽站台,并在站台上停留时间超过5S,视为找到平台。从入水到寻台成功的时间记录为逃避潜伏期。如果小鼠在60s 内没有寻找到平台,将会引导其至平台上并驻留10s,逃避潜伏期记录为60s。计算每天4次逃避潜伏期的平均值为平均逃避潜伏期。
- 记忆保持测试期:在第6天的空间探索实验中,水下的平台被撤去,选择平台对面的象限作为入水点,记录小鼠在60s内穿越原平台位置的次数为穿越平台次数,作为反映小鼠空间记忆能力的指标。
-
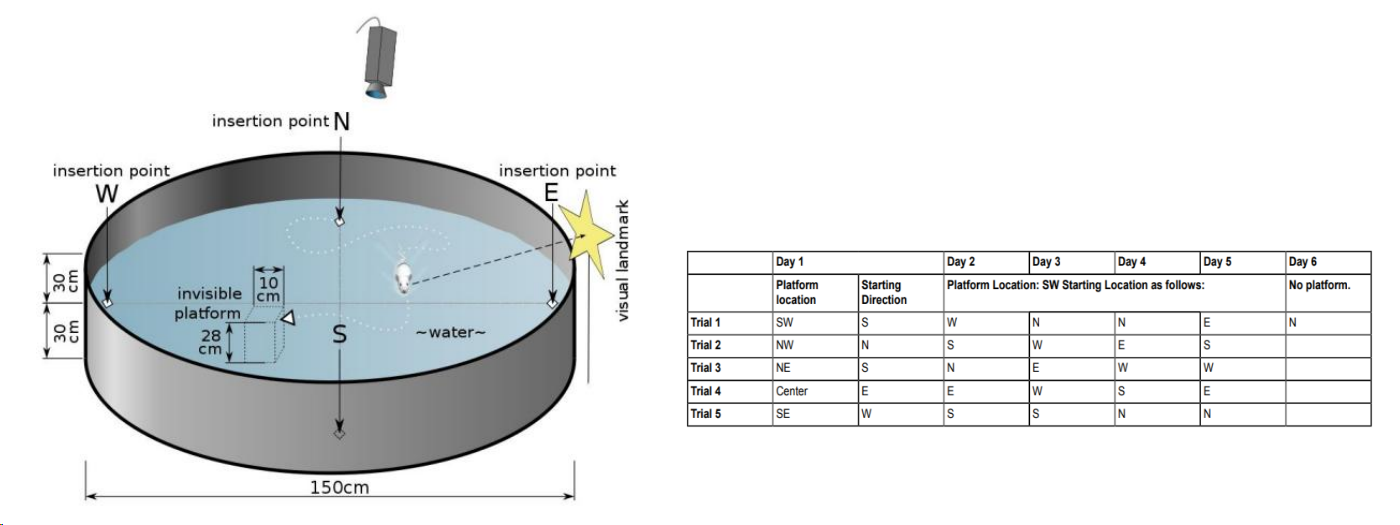
Morris 水迷宫验证模型
避暗实验验证模型:避暗实验分为三个阶段。
-
- 适应期:每只小鼠放进明箱后先适应5min,可在明暗箱之间自由活动。
- 训练期期间,小鼠(四肢)完全进入暗箱后,立即将中门关上,并给予一次电击。电击后让小鼠在暗箱内停留10s,使小鼠形成暗箱与电击之间的联系。将实验小鼠放回原笼。
- 记忆保持测试期,小鼠电刺激训练结束1h和24h后,小鼠放回明箱,中门打开,不给电击。
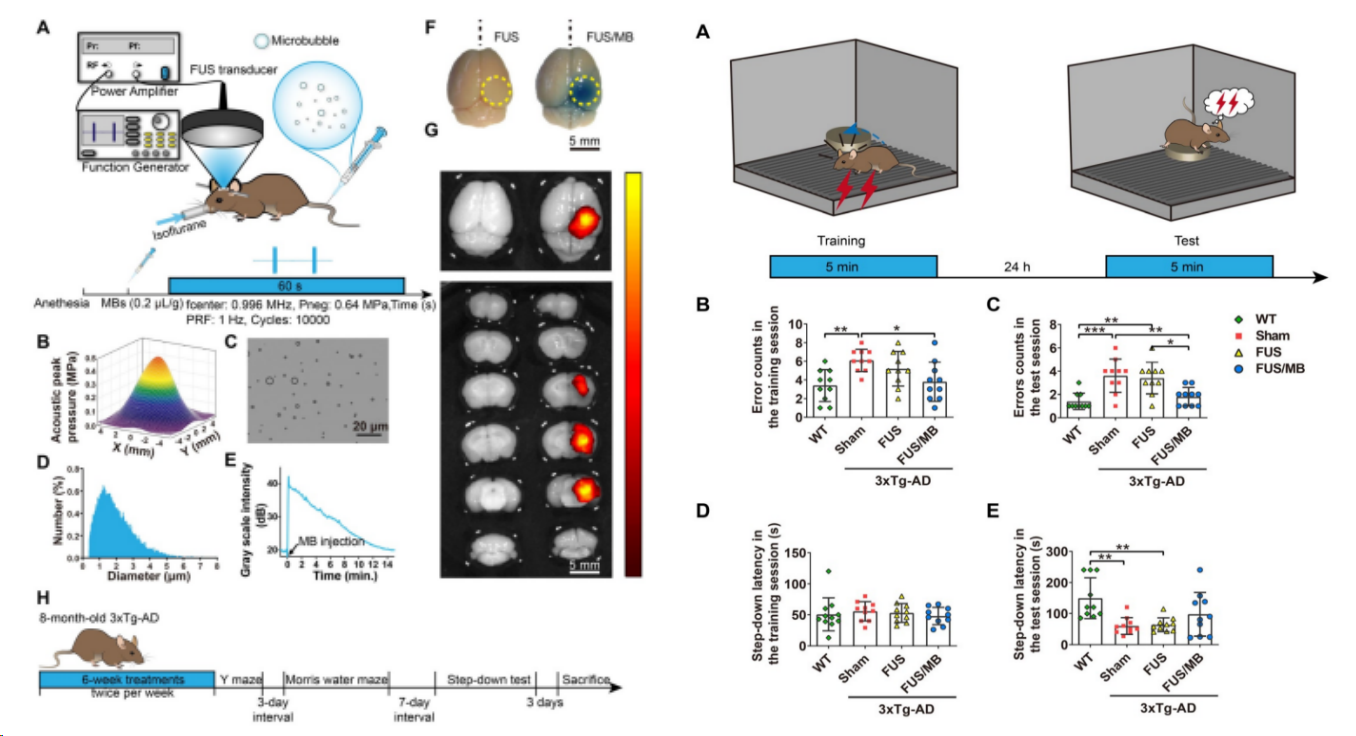
录像系统和图像分析系统记录数据
避暗潜伏期:小鼠第一次进入暗箱并被电击的时间。3min 内未进入暗室的小鼠其潜伏期按180s。计算潜伏期越长,反映动物记忆越好。
避暗错误次数:3min内,小鼠总共进入暗箱并被电击的次数。
五、勋博生物AD模型不同模型的优缺点对比
| 模型类型 | 代表性模型 | 优点 | 缺点 |
|---|---|---|---|
| 转基因 | 5xFAD小鼠 | 病理全面(Aβ沉积、神经元死亡)、发病早 | 基因表达不稳定,缺乏血管病变 |
| 化学诱导 | Aβ海马注射 | 造模快(1-2周)、成本低 | 个体差异大,无NFTs形成 |
| 手术损伤 | 颈动脉结扎 | 模拟血管性痴呆机制 | 死亡率高,病理不特异 |
| 自然衰老 | 老年猕猴 | 自发AD病理,最接近人类 | 时间长(>15年),难以普及 |
六、勋博生物AD模型未来方向
非人灵长类基因编辑模型:利用CRISPR/Cas9技术构建携带APOE4或Tau突变的猕猴,更精准模拟人类AD病理。
复合模型开发:
-
- MODEL-AD计划:整合40+种遗传风险变异小鼠模型,结合PET/MRI进行多模态表征。
- 环境因素整合:睡眠剥夺+转基因模型,研究可干预风险因素。
类器官与干细胞模型:人源iPSC分化的脑类器官,用于研究神经元-Aβ相互作用,弥补动物模型转化瓶颈。
替代模型优化:斑马鱼中表达人类APP和BACE1,用于高通量药物筛选。
