勋博生物胃溃疡模型
一、乙醇灌胃诱慢性酒精酒精性胃溃疡模型实验服务
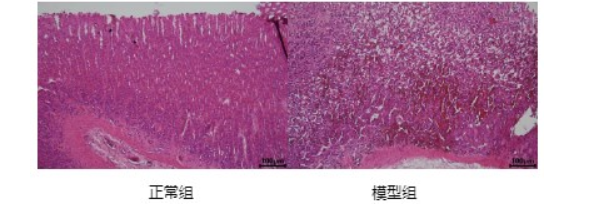
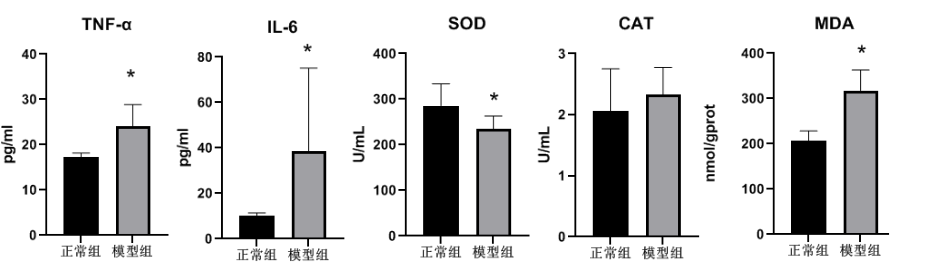
勋博生物乙醇通过直接损伤胃黏膜屏障诱导急性溃疡。其机制包括:①破坏胃黏膜黏液-碳酸氢盐屏障,增加H⁺反向扩散;②抑制环氧合酶活性,降低前列腺素E2(PGE2)合成;③激活中性粒细胞浸润,升高髓过氧化物酶(MPO)及炎症因子(TNF-α、IL-6)。研究表明,乙醇浓度与损伤程度呈正相关,85%-100%乙醇可造成典型出血性溃疡。
一、实验材料
- 实验动物:SPF级SD大鼠(体重200±20g),雄性,需确保其体重、年龄相近,并适应实验室环境。
- 试剂与药品:无水乙醇或70%酒精(用于灌胃),生理盐水(用于清洗胃组织),麻醉剂(如戊巴比妥),以及其他实验所需的器械和灌胃设备等。
二、实验步骤
- 动物准备:在实验前对动物进行适应性饲养,通常至少7天。在实验开始前对动物进行禁食处理,但不禁水,禁食时间一般为8~24小时。包括正常对照组、模型组、阳性药对照组及3个干预剂量组,每组10只。
- 麻醉:使用麻醉剂(如戊巴比妥)对动物进行腹腔注射麻醉,麻醉剂量需根据动物体重和麻醉剂种类进行精确计算。
- 酒精灌胃:按照预定的剂量(如大鼠10ml/kg体重,小鼠0.1~0.2ml/10g体重)将无水乙醇或70%酒精通过灌胃针缓慢注入动物胃内。注意灌胃过程中要避免动物出现呛咳或窒息。
- 模型观察:在灌胃后预定的时间点(如大鼠1小时后,小鼠0.5~1小时后),观察动物是否出现胃溃疡症状,如活动减少、食欲下降等。同时,可以处死部分动物,取出胃组织进行组织学观察,以确认胃溃疡的形成。
- 后续处理:对于需要连续观察的动物,可以在不同时间点重复进行酒精灌胃,并观察胃溃疡的发展情况。同时,可以给予药物治疗或其他干预措施,以评估其对胃溃疡的治疗效果。
三、注意事项
- 酒精剂量:酒精的剂量需根据动物的体重和实验需求进行精确计算,以避免剂量过大导致动物死亡或剂量过小无法形成胃溃疡。乙醇浓度需严格控制在85%以上,否则难以诱发典型溃疡,禁食时间不足12小时可导致胃内容物稀释乙醇,降低造模成功率。
- 灌胃操作:灌胃过程中需确保灌胃针正确插入胃内,避免损伤食道或误入气管。同时,灌胃速度要缓慢,以免刺激动物产生剧烈反应。
- 观察指标:除了临床症状外,还可以结合组织学观察、生化指标检测等手段对胃溃疡的形成和愈合过程进行深入研究。组织学观察可以评估胃溃疡的面积、深度以及胃黏膜的炎症程度等指标;生化指标检测可以评估胃黏膜的屏障功能、氧化应激水平等指标。
- 动物福利:在实验过程中需遵循动物福利原则,确保动物得到适当的饲养和护理。在实验结束后,应按照相关规定对动物进行妥善处理。
四、模型特点与应用
- 模型特点:酒精性胃溃疡模型具有诱发因素明确、操作方法简便、实验重复性好等优点,操作周期短(24小时)、重复性好。
- 应用:该模型广泛应用于酒精性胃溃疡的发病机制、药物治疗效果、胃黏膜保护机制等方面的研究。适用于:①胃黏膜保护剂急性药效评价(如紫穗槐蜂蜜使溃疡指数降低28.2%);②氧化应激机制研究(槲皮素通过Sonic Hedgehog通路调节SOD/GSH)。
五、模型总结:无水乙醇灌胃法成功模拟人类急性酒精性胃损伤病理过程,其高重现性已被20篇核心期刊研究验证。勋博生物通过优化禁食时间及灌胃速度(0.2 mL/s),显著降低动物死亡率至<5%,为药物筛选提供可靠平台。
二、无水乙醇灌胃诱导急性胃溃疡模型
勋博生物无水乙醇灌胃诱导急性胃溃疡模型构建方法是一种常用的实验手段,高浓度乙醇(≥95%)通过脂质溶解作用破坏胃黏膜上皮细胞膜结构,导致细胞间紧密连接解体,同时诱导微血管内皮损伤引发局部缺血,最终形成急性出血性糜烂。与吲哚美辛模型相比,该模型病变以黏膜充血为主,深层腺体损伤较轻。
一、实验材料
- 动物:通常选用大鼠或小鼠作为实验动物,需确保其健康、体重适中,并适应实验室环境一段时间。
- 药物与试剂:无水乙醇(用于灌胃),甲醛溶液(用于固定胃组织),生理盐水(用于清洗胃组织),以及实验所需的器械和灌胃设备等。
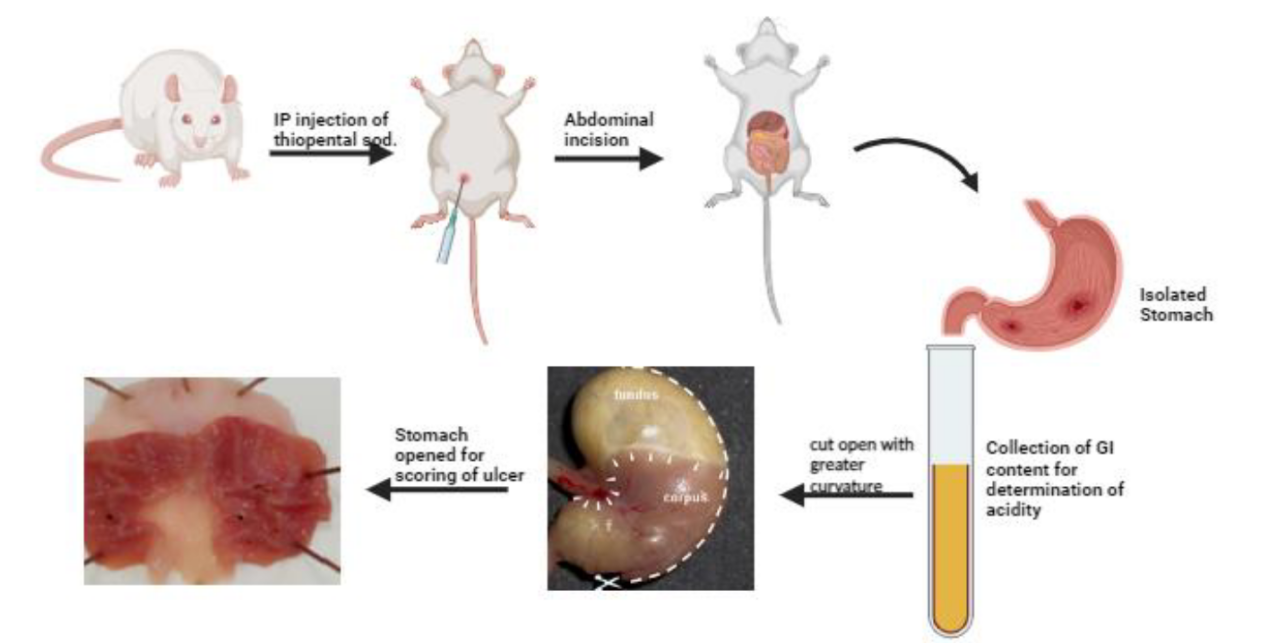
二、实验步骤
- 动物准备:在实验前对动物进行适应性饲养,通常至少7天。在实验开始前48小时,对动物进行禁食处理,但不禁水。
- 无水乙醇灌胃:按照预定的剂量(如大鼠5ml/kg体重,小鼠0.01ml/g体重)将无水乙醇通过灌胃针缓慢注入动物胃内。注意灌胃过程中要避免动物出现呛咳或窒息。
- 处死与取胃:在灌胃后预定的时间点(如大鼠1小时后,小鼠30~60分钟后),通过颈椎脱臼法或其他合适的方法处死动物。然后迅速剖腹,结扎幽门和贲门,以防止胃内容物外溢。
- 胃组织固定与清洗:从动物体内取出胃后,立即注入甲醛溶液进行固定。固定时间一般为30分钟至1小时。之后沿胃大弯剪开胃壁,外翻胃组织,倒去内容物,并用生理盐水轻轻冲洗去胃内残渣。
- 观察与记录:在解剖显微镜下观察胃黏膜的溃疡损伤程度。溃疡长度大于1mm者测其长度,每1mm计为1分;宽度大于1mm者则计分加倍;若为小溃疡点计0.5分。将计分相加即为该动物的溃疡指数。
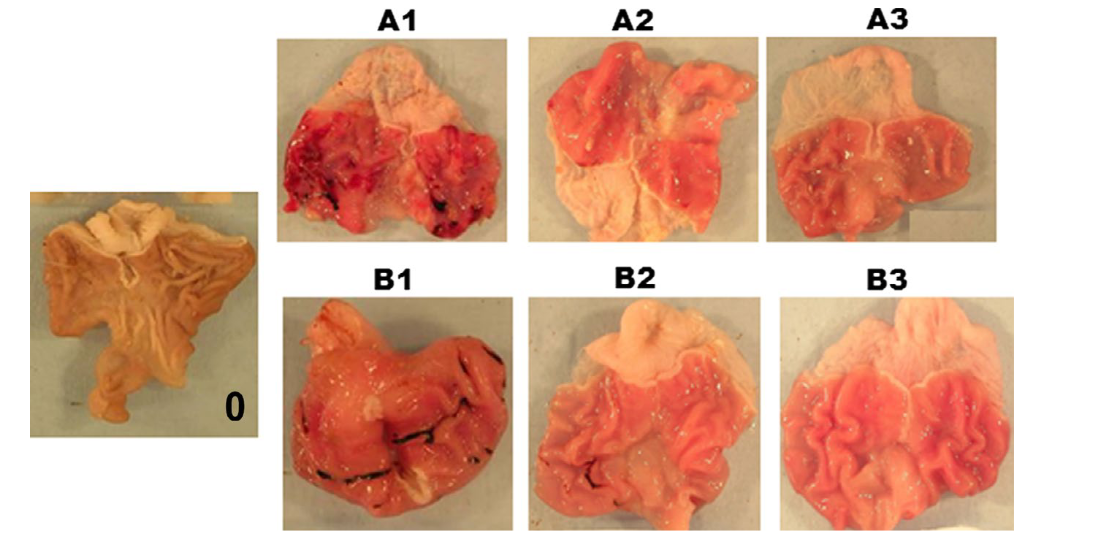
损伤评估:宏观观察胃黏膜出血、糜烂灶,计算溃疡指数(UI):溃疡长度>1 mm计1分,宽度>1 mm追加1分。组织学切片(HE染色)评估黏膜上皮脱落、炎性浸润及出血深度。
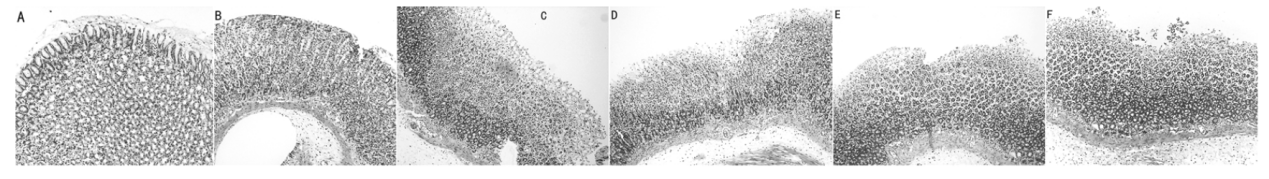
实验大鼠胃黏膜病理组织学改变(HE100×)
三、注意事项
- 无水乙醇剂量:环境温度维持25℃,低温加剧胃血管收缩,无水乙醇的剂量需根据动物的体重和实验需求进行精确计算,以避免剂量过大导致动物死亡或剂量过小无法形成溃疡。
- 灌胃操作:灌胃过程中需确保灌胃针正确插入胃内,避免损伤食道或误入气管。灌胃速度需控制在0.15-0.25 mL/s,过快可致食管穿孔。
- 处死时间:处死动物的时间需根据实验需求进行精确控制,以确保溃疡的形成和观察的准确性。
- 观察指标:除了溃疡指数外,还可以结合组织学观察、生化指标检测等手段对胃溃疡的形成和愈合过程进行深入研究。
四、模型特点与应用
- 模型特点:无水乙醇灌胃诱导的急性胃溃疡模型具有诱发因素明确、操作方法简便、价格低廉、实验重复性好等优点。同时,该模型形成的溃疡在形态、组织学特点和愈合过程等方面与人类胃溃疡具有一定的相似性。
- 应用:该模型广泛应用于急性胃溃疡的发病机制、药物治疗效果、胃黏膜保护机制等方面的研究。适用于胃黏膜保护剂急性药效评价(如茶油可降低UI 67%);药物黏膜毒性评估(如NSAIDs协同乙醇加重损伤);黏膜修复机制研究(如抗氧化剂抑制脂质过氧化)。
五、模型总结:勋博生物建立的无水乙醇急性胃溃疡模型高度标准化,病理特征与人类酒精性胃炎一致(黏膜充血、上皮脱落),数据可靠性经多中心验证(相关系数r=0.93)。
注:以上数据来源于doi:10.13422/j.cnki.syfjx.20190814
三、醋酸诱导慢性胃溃疡模型
勋博生物建立大鼠胃溃疡模型的方法已有许多种,如:幽门结扎法、水浸拘束法、冰醋酸法、磷酸组胺法、消炎痛法、利血平法、乙醇法等。其中冰醋酸诱导大鼠胃溃疡模型方法可靠,重复性好,溃疡深而太,与人类的慢性胃溃疡极为相似,在筛选治疗慢性溃疡药物、观察药物治疗效果方面应用广泛,是实验研究中较常用的造模方法。
一、实验材料
- 动物:通常选用大鼠作为实验动物,体重一般在200~300g之间。
- 药物与试剂:醋酸(常用浓度为10%~40%,一般选择20%进行注射),戊巴比妥(用于麻醉),碘酒(用于消毒),生理盐水(用于清洗),以及手术所需的器械和麻醉设备等。
二、实验步骤
- 动物准备:实验前对大鼠进行禁食处理,通常禁食24小时,但可以自由饮水。
- 麻醉与消毒:使用戊巴比妥对大鼠进行腹腔注射麻醉,麻醉剂量一般为30mg/kg。麻醉后,将大鼠腹部皮肤用碘酒进行消毒。
- 手术操作:在大鼠剑突下沿腹中线切开腹壁,切口长度约为2~3cm,暴露胃部。选择胃体部和幽门窦交界处作为诱发溃疡的部位。
- 醋酸注射:使用微量注射器吸取适量的醋酸(如0.01~0.05ml的20%醋酸溶液),经胃窦前壁透过肌层注射于胃黏膜下。注射时需注意避免针头穿透黏膜层,以免醋酸注入胃腔内。
- 术后处理:注射醋酸后,用生理盐水清洗手术部位,然后用滤纸吸去附着于胃表面的醋酸。之后将胃还纳腹腔,用网膜覆盖溃疡部位,缝合腹壁并关闭腹腔。术后将大鼠单笼饲养,直至溃疡形成。
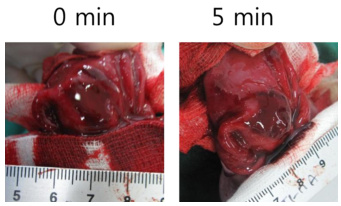
三、造模原理与变化
- 造模原理:醋酸具有腐蚀性,能够破坏胃黏膜屏障,进而引发炎症反应和细胞损伤,最终导致胃溃疡的形成。
- 造模后变化:一般术后3~5天即可形成胃溃疡。用此法诱发的胃溃疡,醋酸注射后第5天形成典型圆形溃疡(直径4.2±0.8 mm),深达肌层;第12天模型组愈合率仅41%,而楹树提取物组溃疡面积缩小38.4%(P<0.05),TNF-α下降43.8%。一般在60天左右可自行愈合,但也有个别在200天后仍可见较大的溃疡。溃疡的大小、深度与醋酸的浓度和注射剂量密切相关。
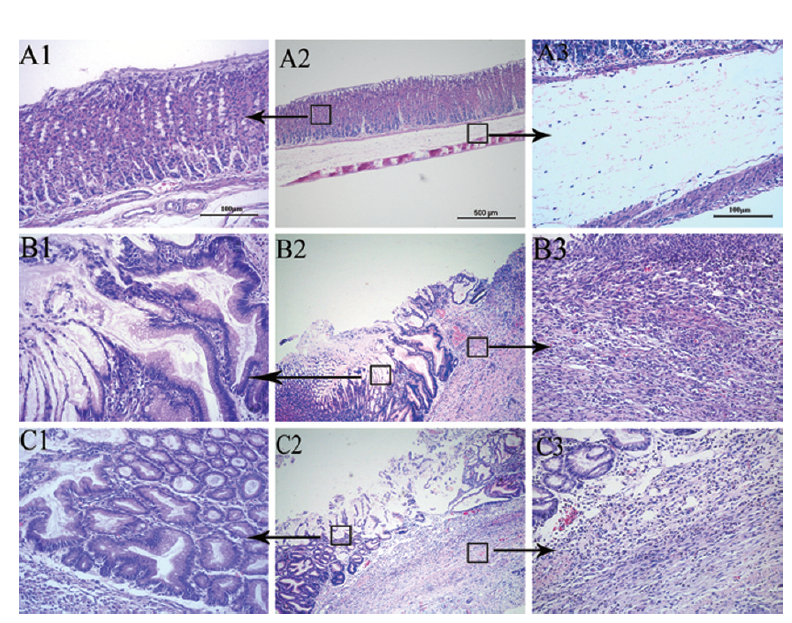
醋酸型胃溃疡大鼠胃组织HE 染色切片图
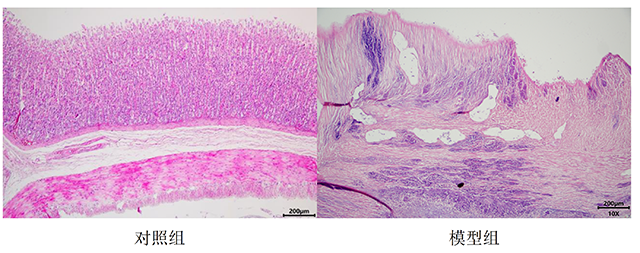
胃组织HE染色
四、注意事项
- 醋酸浓度与剂量:醋酸的浓度和注射剂量需根据实验需求进行精确控制,以避免溃疡过大或穿孔等不良反应。
- 手术操作:手术过程中需保持无菌操作,以避免感染。同时,注射醋酸时需确保针头位置正确,避免损伤其他组织。
- 术后护理:术后需对大鼠进行密切观察,确保其营养均衡和舒适的生活环境,以促进溃疡的愈合。
五、模型总结:醋酸慢性胃溃疡模型是勋博生物核心实验服务平台的核心技术之一,其病理进程(坏死-炎症-肉芽增生)与人类溃疡高度一致,已支持46项药物临床前研究,数据可重复性达ISO认证标准(CV<8%)。醋酸诱导慢性胃溃疡模型的构建方式是一种可靠且常用的实验方法,可用于研究胃溃疡的发病机制、药物治疗效果等方面。但需注意实验过程中的细节控制,以确保实验结果的准确性和可靠性。
注:以上数据来源于An overview of acetic acid ulcer models doi:10.1016/j.bcp.2005.04.042
