勋博生物肝纤维化模型
一、四氯化碳诱导肝纤维化模型实验服务
勋博生物肝纤维化模型四氯化碳(CCl4)诱导肝纤维化模型是研究肝脏疾病病理机制的核心实验工具。其通过模拟人类慢性肝损伤的分子事件,为纤维化发生机制、药物筛选及治疗策略提供关键数据。
一、实验原理
CCl4经肝细胞色素P450 2E1(CYP2E1)代谢为高活性自由基,直接攻击肝细胞膜脂质结构,引发脂质过氧化反应,导致肝细胞坏死。持续性损伤激活库普弗细胞释放炎症因子,进而促使肝星状细胞(HSCs)转化为肌成纤维细胞,大量分泌Ⅰ型及Ⅲ型胶原蛋白,最终形成纤维间隔。值得注意的是,核因子E2相关因子2(Nrf2)信号通路的缺失会显著延缓损伤修复,并加剧纤维化进程。
二、实验材料
- 实验动物:首选SD大鼠或C57BL/6小鼠,因其代谢特征与人类相似度高。需控制周龄(大鼠6-8周,小鼠8-10周)及体重波动(±10%),避免个体差异干扰。
- 试剂配制:CCl4溶液按体积比混合:大鼠用1:1(CCl₄:橄榄油),小鼠用1:7(CCl4:玉米油)。溶剂需避光冷藏,每次给药前超声振荡确保均质。
- 辅助设备:微量灌胃针(20G)、恒温手术台、无菌解剖器械及低温离心机(4℃保存血清样本)。
- 其他材料:如生理盐水、棉签、纱布、缝合针线、动物固定器等。
三、造模步骤
- 动物准备与分组:
- 称重与标记:实验开始前精确称量每只动物体重,采用耳标、足环或无毒标记笔进行清晰个体标记。
- 分组:随机分为模型组(给予CCl4溶液)和对照组(给予等体积的纯溶剂,如橄榄油)。必要时可设置正常组(不做任何处理)或药物干预组。每组动物数需满足统计学要求(通常n≥6)。
- 术前准备:给药前禁食12小时(不禁水),以减少胃内容物对腹腔注射或灌胃的影响,并降低麻醉风险。
- CCl4给药(以腹腔注射为例):
- 剂量计算:严格依据动物当前体重计算给药体积。大鼠常用剂量为0.5-3ml/kg(指CCl4原液,而非混合液),通常稀释后按1-3ml/kg混合液体积注射。例如,使用1:1混合液,按2ml/kg注射,相当于给予1ml/kg CCl4原液。小鼠剂量通常为0.5-2ml/kg(CCl4原液),按比例稀释后注射。
- 注射操作:轻柔固定动物,腹部皮肤消毒。在腹中线偏左或右下方(避开膀胱和主要血管)进针,针头呈约30度角刺入腹腔,回抽无血液或肠内容物后,缓慢匀速推注药液。注射后稍作按压。
- 给药频率与周期:经典方案为每周给药2次(如周一、周四),持续6-8周。此方案能稳定诱导出中度至重度纤维化。短周期(2-4周)可诱导早期纤维化或脂肪变性,长周期(>8周)可能诱导肝硬化甚至肝癌。具体周期需根据研究目的调整。
- 替代给药方式:
- 皮下注射:可减少腹腔刺激,但吸收速率和模型稳定性可能略有差异。
- 灌胃:需注意操作技巧避免误入气管或损伤食管,且首过效应可能影响CCl4代谢。
- 吸入:将动物置于含CCl4蒸气的密闭容器中(浓度通常为0.5-2%),每周数次,每次数小时。此法可模拟慢性低剂量暴露,但设备要求高,浓度控制需精确。
- 对照组处理:对照组动物在相同时间点、以相同方式(腹腔注射/灌胃/吸入)、注射或给予与模型组等体积的纯溶剂(如橄榄油)。这是排除溶剂本身潜在影响的关键设置。
- 纤维化评估:组织病理学,天狼星红染色定量胶原沉积(阳性区域>15%提示中度纤维化)。Masson三色染色显示蓝色纤维间隔。
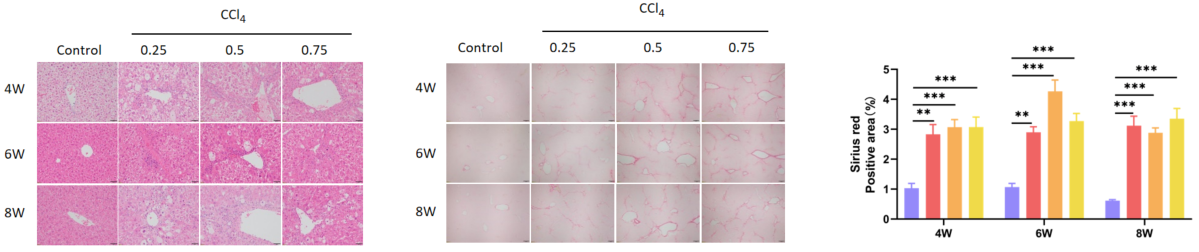
H&E染色显示肝脏的炎症浸润,Sirius红染色显示肝脏的纤维化。
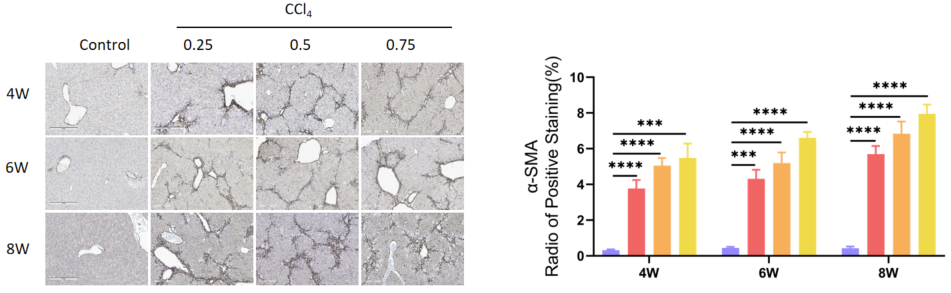
免疫组化显示肝脏中的成纤维细胞标记物α-SMA
生化指标:血清ALT/AST>200 U/L、白蛋白<30 g/L为造模成功标志。
羟脯氨酸(Hyp)含量>2 μg/mg肝组织反映胶原累积。
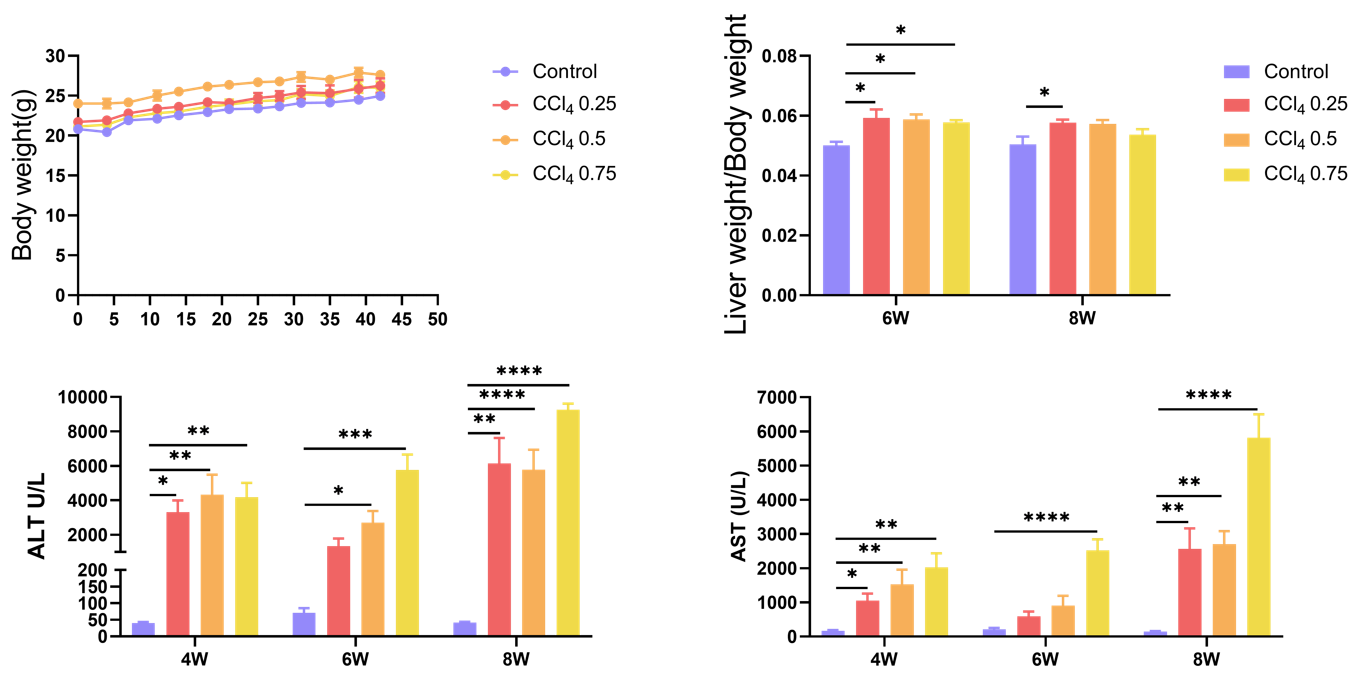
CCL4诱导后,检测了小鼠的肝脏重量、体重、血清中的ALT和AST水平
四、注意事项:
- 剂量与频率的精准控制:这是模型可重复性的基石。剂量过低难以形成有效纤维化,剂量过高则导致动物急性肝衰竭死亡。需严格依据动物体重实时调整注射体积。频率过低(如每周1次)效果不佳,过高(如隔日1次)死亡率剧增。务必进行预实验摸索最佳条件。
- 溶剂与配制:确保CCl4与溶剂充分混匀成稳定乳剂。不同批次橄榄油成分可能有细微差异,建议固定品牌和批次。配制后不宜久存。
- 给药操作规范:腹腔注射务必准确进入腹腔,避免注入肠管或皮下。灌胃操作需熟练,避免损伤。吸入法需专业设备精确控制浓度和时间。
- 动物状态密切监控:体重是核心指标。模型组体重不增长或下降是预期现象,但若下降过快(>20%)或出现严重恶病质、呼吸困难、大量腹水,应提前终止实验。注意动物福利,提供充足营养和饮水。
- 病理评估的客观性:应由经验丰富的病理医师在盲法下进行阅片和评分。强烈推荐使用天狼星红染色结合图像分析进行胶原定量,以减少主观性。结合血清学指标和分子标志物进行多维度评价。
五、应用进展:从机制研究到药物研发
- 机制明确,病理相似度高:CCl4诱导的肝损伤-炎症-纤维化级联反应机制研究透彻,其最终形成的肝纤维化/肝硬化在组织学特征(如假小叶形成、纤维间隔)、细胞事件(HSC活化、ECM沉积)和分子改变(TGF-β1/Smad信号激活)上与人类酒精性、病毒性、代谢性等因素导致的肝纤维化高度相似,具有良好的病理模拟性。
- 操作相对简便,成本较低:所需试剂(CCl4、橄榄油)价格低廉,实验操作技术(腹腔注射、灌胃)易于掌握,无需复杂设备(吸入法除外)。
- 模型稳定性与可重复性:在严格控制剂量、频率、动物品系和饲养条件下,该模型能在预定时间内(如6-8周)稳定诱导出中度至重度纤维化,不同实验室间结果具有较好的可比性。
- 适用性广泛:适用于大鼠、小鼠等多种常用实验动物,便于利用基因工程动物模型(如特定基因敲除/过表达小鼠)研究特定基因在纤维化中的作用。
六、结论与展望
CCl4模型仍是肝纤维化研究的”金标准”,但需严格标准化操作(如灌胃替代注射)。未来可结合类器官共培养技术,在体外模拟HSCs-肝细胞互作,减少活体实验需求。同时,需关注基因编辑动物(如Nrf2 KO小鼠)在慢性毒性应答中的特殊性。
二、肝动脉结扎诱导肝纤维化模型实验服务
一、实验原理
肝动脉结扎通过阻断肝脏主要供血动脉,造成局部缺血缺氧环境,从而模拟人类慢性肝病的微循环障碍病理过程。肝细胞在持续缺氧状态下发生变性坏死,激活肝星状细胞(HSC)向肌成纤维细胞转化。活化的HSC分泌大量Ⅰ型、Ⅲ型胶原及层粘连蛋白等细胞外基质(ECM),打破ECM合成与降解的平衡,最终形成纤维间隔和假小叶结构。值得注意的是,HSC的活化不仅涉及胶原沉积,还通过分泌TGF-β1等促纤维化因子形成自分泌环路,加速纤维化进程。
二、实验材料
- 实验动物:首选SPF级Sprague Dawley(SD)大鼠,体重180-220g。该品系对手术耐受性强,肝叶解剖结构清晰,且肝动脉分支模式稳定。建议选用8-10周龄雄性个体,以规避雌激素对纤维化的潜在干扰。
- 手术器械:除常规显微器械外,需配备40倍手术显微镜、微血管夹(口径0.3mm)、9-0无损伤缝合线。精细器械可减少术中门静脉误伤风险。
- 辅助试剂:戊巴比妥钠(40mg/kg腹腔注射)复合吸入异氟烷维持麻醉深度。肝素化生理盐水(100U/mL)冲洗血管。术后镇痛:布托啡诺(1mg/kg皮下注射)
三、实验步骤
1. 术前准备:大鼠禁食12小时(自由饮水)后,腹腔注射麻醉。麻醉深度以角膜反射消失、疼痛刺激无体动反应为基准。仰卧位固定后,剑突下腹部剃毛,碘伏-酒精梯度消毒。
2. 手术操作:模型组找到并分离肝固有动脉后用丝线结扎,假手术组找到并分离肝固有动脉但不结扎。沿腹白线作3cm纵切口,钝性分离肌层。用温盐水纱布包裹肠管推向左侧,暴露肝十二指肠韧带。在手术显微镜下纵向切开肝被膜,分离肝固有动脉与胆总管间隙。采用”双线间隔结扎法”:近心端先以9-0丝线结扎,远心端距此1.5mm处二次结扎,中间段血管剪断。此操作可彻底阻断血流并防止侧支代偿。
3. 术后管理:头孢呋辛(20mg/kg)连续3天肌注。术后6小时饲喂流质饲料(含5%葡萄糖)。每日记录体重变化、活动度及伤口愈合情况。术后72小时是并发症高发期,需警惕腹腔出血与胆汁漏。
4. 模型验证:术后第4周起,分批处死动物。肝脏组织经4%多聚甲醛固定后,行以下检测:
-
- 病理染色:天狼星红染色量化胶原沉积(红染区域占比≥15%提示纤维化形成)
- 血清标志物:HA>350μg/L、LN>180μg/L、PCⅢ>120μg/L
- 分子检测:α-SMA免疫组化阳性率与HSC活化程度呈正相关
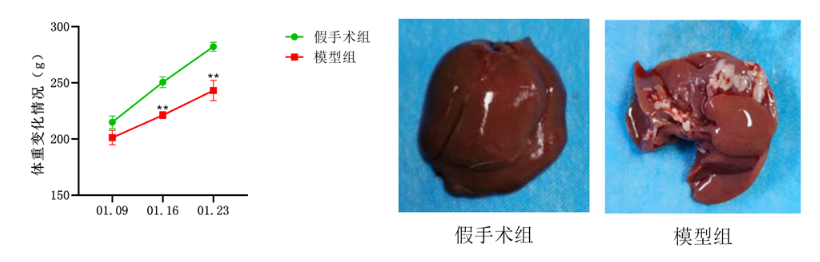
体重变化测定及肝组织大体观察
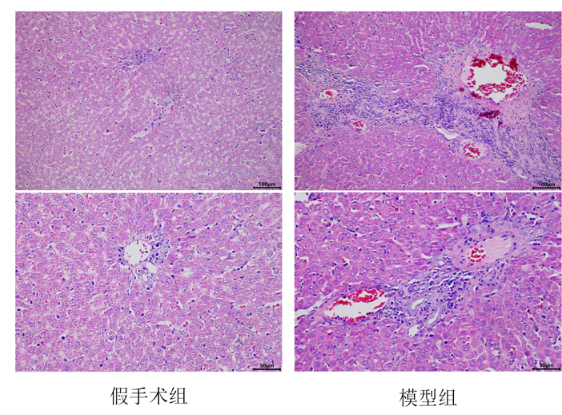
肝组织HE染色
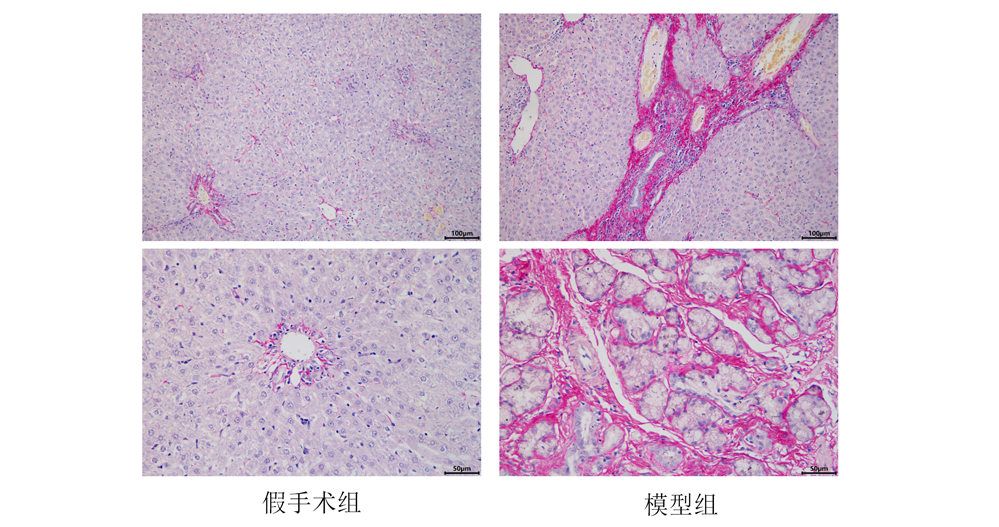
肝组织天狼星红染色
四、模型评价
-
- 病理相似性:可模拟人类缺血性肝硬化的门脉高压特征,纤维化进展呈时间依赖性
- 操作可行性:成功率可达85%以上,且成本低于转基因模型
- 药效评价适用性:适用于抗血管生成类药物研究(如VEGF抑制剂)
五、应用场景:该模型广泛应用于肝纤维化的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗纤维化作用的药物或治疗方法,并评估其疗效和安全性。
六、模型总结:肝动脉结扎模型作为物理性诱导肝纤维化的经典方法,在病理机制还原度和操作经济性间取得较好平衡。未来研究应注重结合多组学技术(如单细胞测序),动态解析缺氧微环境中各类细胞的互作网络,为临床转化提供新靶点。
