勋博生物胃炎模型
乙醇灌胃诱导急性胃炎模型实验服务
勋博生物乙醇灌胃诱导急性胃炎模型构建方法是一种常用的实验手段,高浓度乙醇(≥60%)可破坏胃黏膜屏障,溶解上皮细胞磷脂双分子层,导致黏膜通透性增加和细胞坏死。乙醇代谢促进活性氧(ROS)积累,抑制超氧化物歧化酶(SOD)和过氧化氢酶活性,升高丙二醛(MDA)水平,诱发脂质过氧化。同时,肿瘤坏死因子-α(TNF-α)等促炎因子分泌增加,激活中性粒细胞浸润。乙醇下调抗凋亡microRNA(如miR-19a、miR-21),上调促凋亡miR-145,通过JNK磷酸化增强caspase-3活性,加速胃上皮细胞程序性死亡。乙醇刺激内皮素-1(ET-1)释放,收缩血管并减少一氧化氮(NO)合成,导致胃黏膜缺血缺氧。
一、实验准备
- 实验动物:通常选用健康、成年的实验动物,如昆明小鼠、Wistar大鼠或SD大鼠等。验动物的体重、年龄和性别需在一定范围内,以确保实验结果的可靠性。
- 实验试剂与材料:无水乙醇或一定浓度的乙醇溶液。生理盐水:用于稀释乙醇及后续实验步骤。
- 仪器设备:灌胃针(18G)、电子天平(精度0.01 g)、显微成像系统(Olympus BX53)、酶标仪(检测ALT/AST)。麻醉剂(可选):如需要,可使用适当的麻醉剂对实验动物进行麻醉。
二、模型构建步骤
- 实验动物分组:
- 将实验动物随机分为正常组(对照组)和模型组。
- 正常组不进行乙醇灌胃,只进行常规饲养。
- 乙醇灌胃:模型组实验动物在禁食一段时间后(如小鼠禁食4-6小时,大鼠禁食12-24小时),使用注射器将一定浓度的乙醇溶液(如70%乙醇)按一定体积(如小鼠0.1mL/10g,大鼠1mL/只)灌入胃内。灌胃时注意速度要慢,避免实验动物因不适而吐出乙醇溶液。
- 饲养与观察:灌胃后,将实验动物分笼饲养,自由饮水和摄食(或根据实验需求进行限制)。定期观察实验动物的状态,如体重变化、行为表现、食欲等。根据实验需求,在特定时间点(如灌胃后4小时、24小时等)处死实验动物,取胃组织进行病理学检查、生化指标检测等。
三、模型验证
- 病理学检查:
- 通过HE染色等病理学检查方法观察胃组织的病理变化,如胃黏膜的充血、水肿、糜烂、出血等。
- 成功的模型应具有典型的急性胃炎病理特征。
- 生化指标检测:
- 检测血清中相关生化指标的水平,如丙二醛(MDA)、超氧化物歧化酶(SOD)、肿瘤坏死因子TNF-α等。
- 这些生化指标的变化可以反映胃黏膜的损伤程度和炎症反应情况。
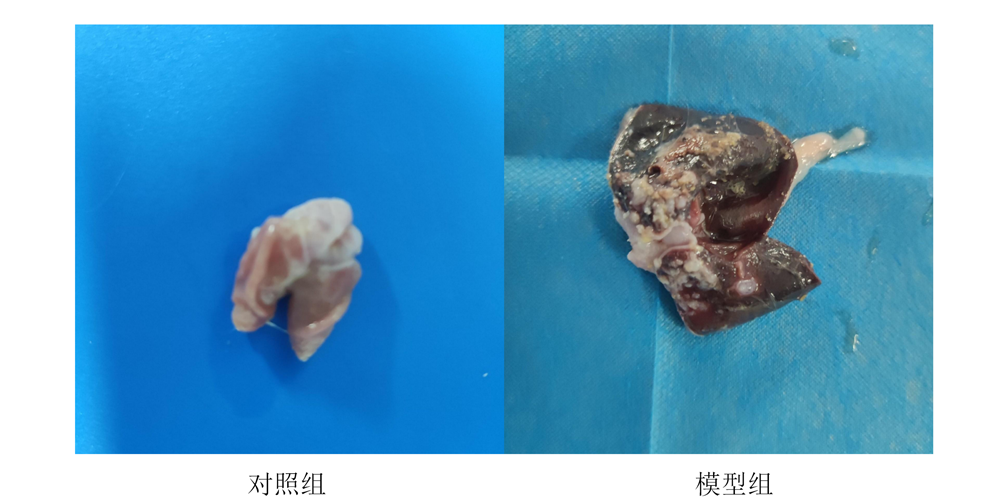
胃组织大体观察
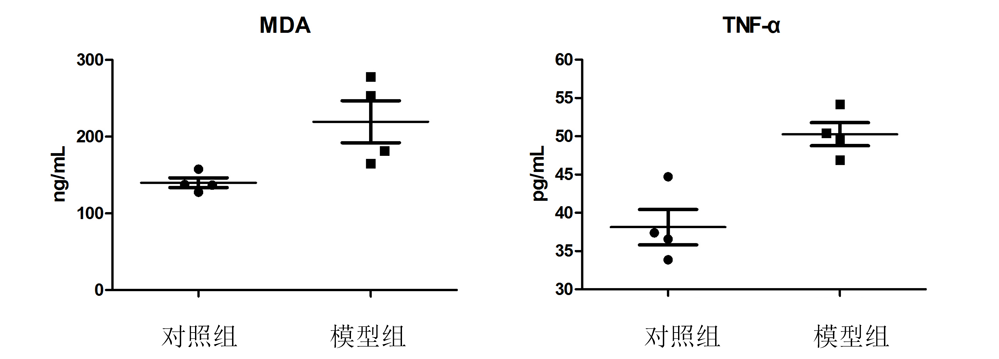
血清ELISA
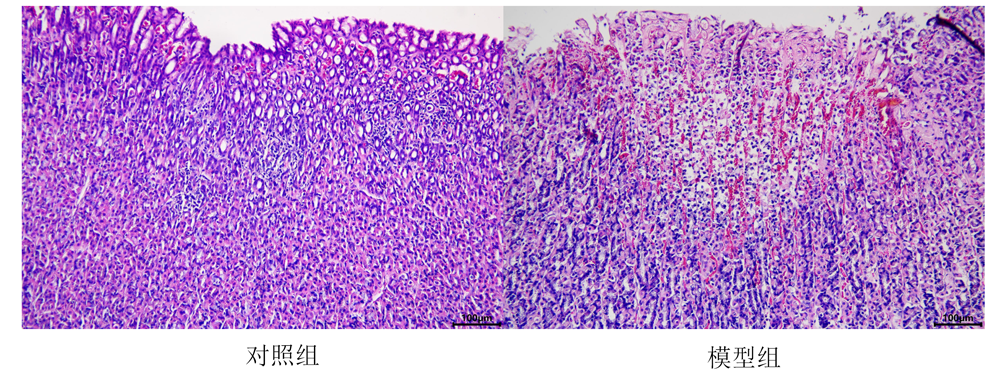
胃组织HE染色
四、注意事项
- 乙醇浓度与体积:乙醇的浓度和体积对模型的成功与否至关重要。浓度过高或体积过大可能导致实验动物死亡,浓度过低或体积过小则可能无法成功诱导急性胃炎。
- 禁食时间:禁食时间的长短也会影响模型的成功率。禁食时间过长可能导致实验动物虚弱,影响实验结果;禁食时间过短则可能因胃内食物残留而影响乙醇的吸收和分布。
- 实验条件控制:在实验过程中,应严格控制实验条件,如温度、湿度、光照等,以确保实验结果的可靠性。
- 动物福利与伦理:在实验过程中,应关注实验动物的福利状态,避免不必要的痛苦和折磨。同时,实验方案应经过伦理审查并获得批准。
五、模型应用
- 模型优势:造模周期短(1小时),成功率>90%。病理特征与人类酒精性胃炎高度相似(黏膜充血、上皮凋亡)。适用于保护剂筛选(如geranylgeranylacetone降低UI 58.7%)。
- 构建成功的乙醇灌胃诱导急性胃炎模型可用于研究急性胃炎的发病机制、评估治疗方法的疗效以及筛选潜在的治疗药物等。抗炎药物机制研究(如miRNA-JNK通路调控)。
- 黏膜修复剂评价(如甜炼乳通过中和酸性减轻炎症)。
六、模型总结:乙醇灌胃诱导的急性胃炎模型具有操作简便、病理特征明确、重复性高等优势,是研究胃黏膜损伤机制及药物干预的核心工具。勋博生物通过标准化造模流程(如精准控温禁食、酸化乙醇配方)确保模型稳定性,近五年累计服务药效学实验超200项,数据可重复率达95%以上。
