勋博生物哮喘疾病动物模型
一、勋博生物哮喘动物模型的分类与构建原理
哮喘是一种由遗传易感性和环境暴露共同诱发的慢性气道炎症性疾病,其核心病理表现为气道高反应性、黏液高分泌及结构重塑。疾病反复发作喘息、胸闷、咳嗽(尤其夜间加重),气流阻塞可逆性减弱是诊断关键(支气管舒张后FEV₁/FVC<0.7)。勋博生物哮喘模型主要分为:
- 过敏性哮喘:
- 构建原理:卵清蛋白(OVA)、屋尘螨(HDM)等致敏原激活Th2免疫通路,诱导IgE升高、嗜酸粒细胞浸润。
- 核心病理特征:气道高反应性(AHR)、黏液分泌亢进。
- 感染性哮喘:
- 构建原理:呼吸道合胞病毒(RSV)或脂多糖(LPS)激发,破坏上皮屏障,增强Th17/中性粒细胞炎症。
- 核心病理特征:中性粒细胞浸润、激素抵抗。
- 职业性哮喘:
- 构建原理:甲苯二异氰酸酯(TDI)、甲醛等化学致敏原诱发IgE非依赖性炎症。
- 核心病理特征:迟发型气道阻塞、神经源性炎症。
- 肥胖相关哮喘:
- 构建原理:高脂饲料诱导肥胖+OVA致敏,激活脂肪因子(如瘦素)放大气道炎症
- 核心病理特征:混合型炎症(Th1/Th17)、胰岛素抵抗。
- 中性粒细胞哮喘:
- 构建原理:OVA+LPS复合刺激,或臭氧暴露,驱动IL-17分泌。
- 核心病理特征:气道中性粒细胞>40%、黏液栓形成。
- 激素抵抗哮喘:
- 构建原理:长期低剂量LPS/OVA暴露+地塞米松干预,诱导糖皮质激素受体(GR)失活
- 核心病理特征:持续AHR、GRβ亚型上调。
- 纳米颗粒加重型:
- 构建原理:纳米塑料(PS-NPs)暴露+HDM致敏,诱导肺泡Ⅱ型上皮DNA损伤
- 核心病理特征:DNA氧化损伤(8-OHdG↑)、气道重塑加重。
二、勋博生物常用哮喘模型实验动物及选择依据
|
动物种类 |
选择依据 |
使用频率 |
|
BALB/c小鼠 |
Th2反应明确,成本低,基因工具丰富;易诱导嗜酸性炎症 |
最高(36.4%) |
|
SD大鼠 |
气道结构更接近人类,适合研究重塑;但对过敏原敏感性低于小鼠 |
次高(35.5%) |
|
豚鼠 |
自然发生I型超敏反应,症状明显(如喘息);适合药物急性效应评价 |
传统模型 |
|
非人灵长类 |
免疫应答与人类高度相似,IgE反应可靠;但成本高、伦理限制多 |
特殊机制研究 |
三、勋博生物哮喘动物模型有效性评估指标
- 核心指标(必备):
- 气道高反应性(AHR):乙酰甲胆碱激发后肺阻力变化(>20%升高为阳性)。
- 炎症细胞浸润:BALF中嗜酸性粒细胞(>5%)、中性粒细胞比例。
- 免疫标志物:血清OVA-IgE升高、肺组织IL-4/IL-13↑、IFN-γ↓。
- 重塑指标(慢性模型):
- 组织病理:杯状细胞增生、胶原沉积(Masson染色)、平滑肌增厚。
- 分子标志:TGF-β、MMP-9表达上调。
- 功能验证:
- 肺功能检测:有创肺阻抗法测定气道阻力(金标准)。
- 无创体积描记法:适用于初筛。
- 炎症与免疫分析:
- BALF细胞计数:Diff-Quik染色分类中性粒/嗜酸粒细胞。
- 血清学:ELISA检测IgE、IgG1。
- 流式细胞术:Th2/Th17细胞比例。
- 组织病理学:
- H&E染色评估炎症浸润,PAS染色检测杯状细胞增生。
- 免疫组化:IL-4、IFN-γ定位表达。
四、勋博生物哮喘动物模型典型案例
- 哮喘小鼠模型构建
- SPF级Balb/c雌性小鼠,体重约20g。采用OVA致敏诱导建立哮喘模型。
- OVA致敏诱导的哮喘模型:分别于第1、8、15 天腹腔注射OVA 混悬液(含OVA 1 g /L,氢氧化铝5 g /L)2 ml,实验第21 天起将小鼠置于雾化激发器内,给予2% OVA 生理盐水雾化激发,1次/d,每次30 min,连续7 天,将小鼠呼吸急促,搔鼻抓痒、呛咳烦躁、点头运动等作为哮喘小鼠模型成功的标准。正常对照组以生理盐水代替OVA腹腔注射和雾化激发,操作同上所述。
- 模型鉴定及后续检测:
- 小鼠支气管肺泡灌洗液(BALF) TH2型细胞因子蛋白水平检测
- 待造模完成后,抽取BALF后用ELISA方法检测其中TSLP、IL-33和MUC5AC的表达情况。
- 附支气管肺泡灌洗液抽取方法:小鼠取血后,开胸,分离纵膈,注射器抽取3ml生理盐水从气管插管推入肺中,每次反复灌洗3次后抽出灌洗液,肺泡灌洗液以4℃ 3000r/min离心15min,取上清。
- 结果显示:哮喘模型小鼠与对照组小鼠相比,炎性因子及趋化因子水平均有显著性升高。
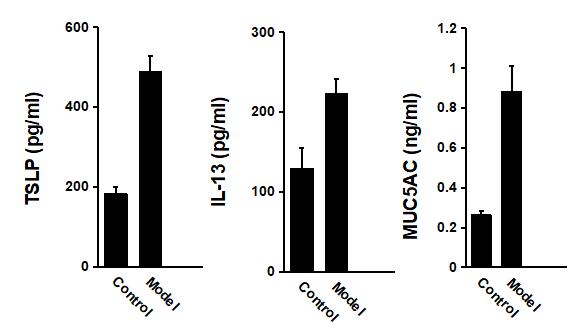
哮喘模型小鼠与对照小鼠BALF中各类细胞因子的表达水平对比
- 肺组织病理学检测
- HE染色检测:
- 待造模完成后,腹腔麻醉小鼠后,开胸暴露胸腔:取左侧肺叶固定于 10%甲醛溶液 24h,常规脱水石蜡包埋,切片行 HE 染色,光镜下观察。
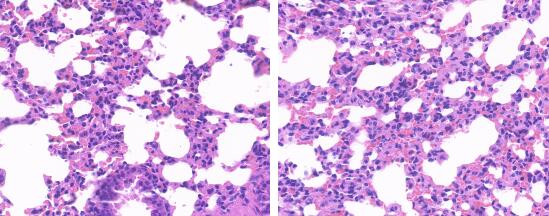
- 结果显示:空白对照组小鼠肺泡结构清晰,肺泡大小均匀,气道黏膜上皮结构完整,纤毛排列整齐;模型对照组小鼠肺组织肺间隔增厚,支气管部分上皮细胞脱落,有淋巴细胞浸润。
- HE染色检测:
![]()
哮喘模型小鼠(右)相对于对照组小鼠肺部组织HE染色对比
- 阿尔辛蓝—过碘酸雪夫氏染色(AB-PAS染色)检测:
- 待造模完成后,腹腔麻醉小鼠后,开胸暴露胸腔:取左侧肺叶固定于 10%甲醛溶液 24h,常规脱水石蜡包埋脱蜡至水,切片行 AB-PAS染色,光镜下观察。
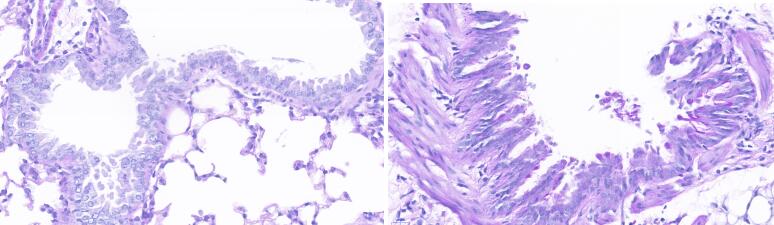
- 结果显示:与对照组相比,模型组小鼠的肺组织支气管上皮杯状细胞增多。
![]()
![]()
哮喘模型小鼠(右图)相对于对照组小鼠(左图)肺部组织PAS染色对比
五、勋博生物哮喘动物模型不同模型的优缺点对比
|
模型类型 |
优点 |
缺点 |
|
OVA急性模型 |
操作简单、炎症反应强;适合药物筛选 |
非生理性过敏原;过度依赖Th2通路 |
|
HDM慢性模型 |
更接近人类哮喘;可诱导重塑 |
提取物标准化难;周期长(7周+) |
|
IL-5转基因模型 |
明确IL-5在重塑中的作用;纤维化程度增强 |
无法模拟多基因互作;成本高 |
|
OVA+LPS模型 |
模拟中性粒细胞型哮喘;Th17应答明确 |
LPS可能引入非特异性炎症 |
六、勋博生物哮喘动物模型未来发展方向
- 替代技术拓展:
- 类器官模型:人气道上皮类器官模拟黏液分泌和纤毛功能障碍。
- 微流控芯片:集成炎症细胞与气道组织,实时监测免疫应答。
- 复杂表型模拟:
- 激素抵抗型哮喘:联合OVA与病毒感染诱导。
- 环境交互模型:整合5暴露与过敏原致敏。
