勋博生物胃肠炎模型
OVA联合卵白蛋白诱导嗜酸性粒细胞性胃肠炎模型实验服务
勋博生物嗜酸性粒细胞性胃肠炎(Eosinophilic Gastroenteritis, EG)是一种以胃肠黏膜嗜酸性粒细胞(EOS)浸润为特征的过敏性疾病。本模型通过卵清蛋白(OVA)联合免疫佐剂氢氧化铝(Al(OH)₃)诱导Th2型免疫应答,激活IL-5介导的EOS分化与迁移通路。IL-5作为关键细胞因子,通过结合EOS表面受体,促进骨髓EOS释放并趋化至胃肠道。同时,OVA经灌胃激发后,抗原穿透肠黏膜屏障,激活肥大细胞释放组胺及IgE,进一步招募EOS浸润并释放主要碱性蛋白(MBP),导致黏膜损伤、上皮增生及组织纤维化。
一、实验准备
- 实验动物:通常选用SPF级Balb/c小鼠,雌性,8周龄左右,体重在一定范围内(如18~22g)。选用该品系因其Th2免疫应答敏感性强,利于过敏模型构建。实验前需对小鼠进行适应性饲养,确保其状态良好。
- 实验试剂与材料:OVA(卵白蛋白):作为致敏原和激发剂。氢氧化铝佐剂:用于增强OVA的免疫原性。生理盐水:用于稀释OVA和氢氧化铝佐剂。1mL注射器:用于腹腔注射和灌胃。
- 其他实验器材:如离心管、抗凝管、显微镜、血细胞分析仪等。
二、实验步骤
- 试剂配置:致敏工作液配置:将OVA溶于氢氧化铝佐剂中,配制成一定浓度(如0.5mg/mL)的致敏工作液,现配现用。激发工作液配置:将OVA溶于生理盐水中,配制成一定浓度(如0.1g/mL)的激发工作液,现配现用。
- 致敏阶段:小鼠分别于第1天和第15天腹腔注射0.1mL致敏工作液。注射时注意无菌操作,避免感染。
- 激发阶段:小鼠分别于第20天、第22天和第24天灌胃0.1mL/只的激发工作液。灌胃前需禁食一段时间(如4~6小时),以确保OVA能够充分与胃黏膜接触并引发免疫反应。
- 样本采集与检测:
- 在第24天致敏后10~12小时,小鼠眼内眦采血100μL抗凝,用于全自动血细胞分析仪检测嗜酸性粒细胞(EOS)数量。
- 在第25天,小鼠麻醉后处死,取血清、胃和肠道(空肠)组织进行病理检测。
- 血清学检测:末次激发后24小时麻醉取血,离心分离血清,ELISA检测IgE、IL-5水平。
- 组织病理学:取胃、空肠及结肠组织,4%多聚甲醛固定,石蜡包埋后切片(5 μm),HE染色评估EOS浸润及黏膜损伤,免疫组化检测MBP表达。
- 外周血分析:抗凝全血经溶血处理后,流式细胞术计数EOS(CCR3⁺/Siglec-F⁺细胞群)。
四、模型验证
- 病理学检查:通过HE染色观察胃和肠道组织的病理变化,如嗜酸性粒细胞浸润、水肿、充血等。成功的模型应具有典型的嗜酸性粒细胞性胃肠炎病理特征。
- 生化指标检测:检测血清中IgE水平的变化。与正常组相比,模型组小鼠的IgE水平应显著升高。
lgE检测
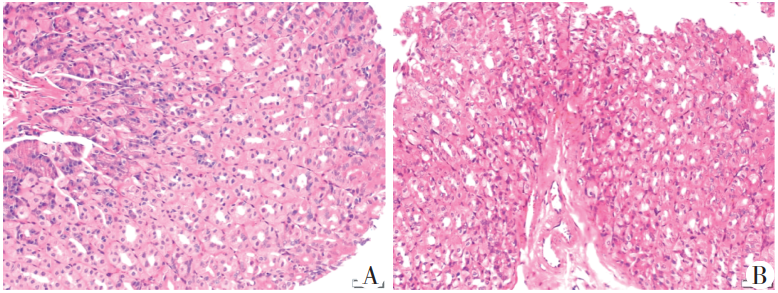
小鼠胃黏膜EOS(HE染色,×200)
A:正常对照组胃窦;B:OVA⁃EG组胃窦
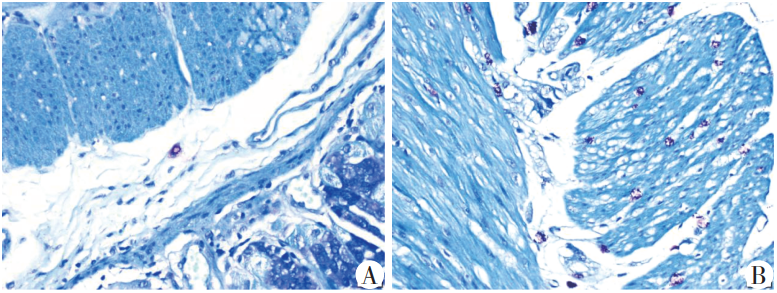
小鼠胃黏膜MC(甲苯胺蓝染色,×200)
A:正常对照组胃窦;B:OVA-EG组胃窦
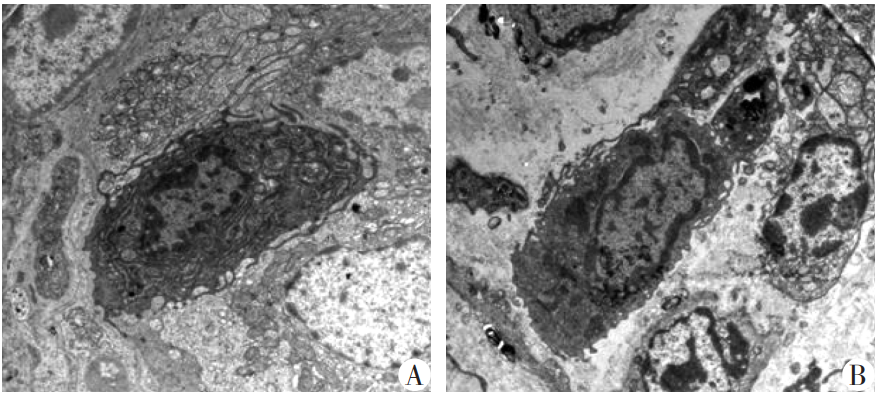
电镜观察两组小鼠胃窦黏膜MC脱颗粒变化(×7000)
A:对照组胃窦;B:OVA-EG组胃窦。
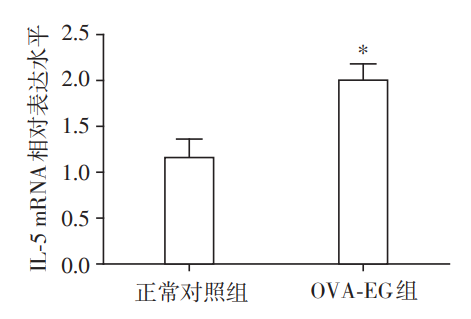
两组小鼠胃窦黏膜组织IL-5 mRNA表达比较
五、注意事项及模型应用
- 无菌操作:在整个实验过程中,应严格遵守无菌操作规程,以防止感染影响实验结果。
- 剂量控制:OVA和氢氧化铝佐剂的剂量对模型的成功与否至关重要。剂量过大可能导致小鼠死亡或产生严重的免疫反应;剂量过小则可能无法成功诱导嗜酸性粒细胞性胃肠炎。
- 实验条件控制:在实验过程中,应严格控制实验条件,如温度、湿度、光照等,以确保实验结果的可靠性。
- 动物福利与伦理:在实验过程中,应关注小鼠的福利状态,避免不必要的痛苦和折磨。同时,实验方案应经过伦理审查并获得批准。
- 适用于抗过敏药物(如IL-5抑制剂、白三烯受体拮抗剂)的药效评价。
- 通过IL-5基因敲除鼠验证EOS浸润的依赖性,或利用eotaxin缺陷鼠研究趋化因子协同作用。
七、模型总结:勋博生物构建的OVA诱导EG模型高度模拟人类疾病特征,包括Th2免疫偏移、EOS特异性浸润及黏膜屏障破坏。其成模率达90%,且通过PLGA包裹抗原提升肠道靶向性,较传统腹腔注射法更贴近食物过敏病理过程。
上述数据来源于doi:10.7655/NYDXBNS20181106
