勋博生物脑膜炎动物模型
一、勋博生物脑膜炎动物模型的分类与构建原理
(一)按病原体类型分类
- 细菌性脑膜炎模型
- 构建原理:通过模拟细菌侵入中枢神经系统(CNS)的途径诱导炎症。分为两类:
- 自然感染途径:鼻腔/腹腔注射细菌(如肺炎球菌、B组链球菌),依赖菌血症突破血脑屏障(BBB)。
- 直接CNS接种:小脑延髓池或脑室内注射病原体(如GBSⅢ),绕过BBB直接引发脑膜炎症,病理进程可控。
- 代表模型:新生SD大鼠小脑延髓池接种GBSⅢ模型(成功率>90%)。
- 病毒性脑膜炎模型
构建原理:通过颅内或中耳接种病毒(如西尼罗河病毒、疱疹病毒),利用病毒嗜神经特性感染脑膜细胞。
- 自身免疫性脑膜炎模型
- 构建原理:注射髓鞘蛋白抗原(如MBP)加佐剂(CFA),诱发T细胞攻击自身CNS组织,模拟多发性硬化症相关脑膜炎。
- 代表模型:豚鼠脊髓-佐剂乳剂模型。
- 结核性脑膜炎模型
- 构建原理:眼球后静脉丛注射结核分枝杆菌H37RV,经血行播散至脑膜,需联合百日咳杆菌增强免疫应答。
(二)按动物发育阶段分类
- 幼龄动物模型(如11日龄大鼠):BBB发育不全,易通过菌血症诱发脑膜炎。
- 成年动物模型:需直接CNS接种,否则发病率低。
二、勋博生物脑膜炎模型常用实验动物及选择依据
- 常用动物模型表格对比
| 实验动物 | 适用模型类型 | 选择依据 | 局限性 |
| SD大鼠 | 细菌性/结核性脑膜炎 | BBB发育与人类婴儿相似;遗传背景清晰;成本低 | 成年鼠自然感染率低 |
| C57BL小鼠 | 结核性/病毒性脑膜炎 | 免疫基因明确;易转基因;适用于耐药性研究 | 脑体积小,操作难度大 |
| 豚鼠 | 自身免疫性脑膜炎 | 对髓鞘抗原敏感性强;炎症反应与人类相似 | 成本高;行为学评估困难 |
| 家兔 | 细菌性/隐球菌性脑膜炎 | 耳缘静脉易穿刺;脑脊液采集方便 | 遗传背景多样性不足 |
| 非人灵长类 | 病毒性/自身免疫性脑膜炎 | 高级脑功能接近人类;免疫系统相似度高 | 伦理限制;成本极高 |
- 选择核心原则
- 解剖相似性(如BBB结构)
- 免疫应答匹配度(如T细胞反应)
- 操作可行性(如幼鼠小脑延髓池穿刺)
三、勋博生物脑膜炎模型有效性评估指标
- 临床与行为学指标
- 生存率/体重损失:>20%体重损失或生存率<50%提示模型成功。
- 神经症状评分(Loeffler/Racine标准):0级:正常;4级:单侧瘫痪;6级:癫痫持续状态。
- 行为学测试:旷场实验(活动减少)、Morris水迷宫(空间记忆障碍)。
- 实验室与影像学指标
| 检测类型 | 关键指标 | 意义 |
| 脑脊液分析 | WBC >1000/μL;蛋白↑;糖↓ | 炎症直接证据 |
| 血液检测 | CRP↑;降钙素原↑;中性粒细胞↑ | 全身炎症反应 |
| 病理学检查 | 血管炎;胶质结节;脱髓鞘;神经元凋亡 | 组织损伤程度 |
| 影像学 | MRI T2加权像脑膜强化;脑室扩大 | 脑水肿/脑萎缩 |
- 分子生物学指标
- 炎症因子:TNF-α、IL-1β在脑脊液中升高。
- 凋亡标志物:Caspase-3阳性细胞率>15%提示神经元损伤。
四、勋博生物脑膜炎模型不同模型优缺点对比
| 模型类型 | 优点 | 缺点 | 适用研究 |
| 细菌性(直接接种) | 病理进程可控(6-24h发病);死亡率>80% | 绕过自然感染途径;免疫应答不完整 | 抗生素药效评估 |
| 细菌性(自然感染) | 模拟真实感染路径;BBB穿透机制研究 | 幼龄动物需求;发病率不稳定(30-70%) | 病原侵袭机制 |
| 自身免疫性(EAE) | 模拟人类脱髓鞘病变;临床分期明确 | 需佐剂增强免疫;个体差异大 | 免疫调节疗法开发 |
| 病毒性(颅内接种) | 神经嗜性模拟精准;可研究潜伏感染 | 操作难度大;生物安全风险高 | 抗病毒药物筛选 |
| 结核性 | 慢性炎症过程真实(4周病程) | 病原培养周期长;死亡率不可控 | 新型诊断标志物验证 |
五、勋博生物脑膜炎模型典型案例:MOG35-55联合百日咳毒素诱导变态反应性脑脊髓炎模型(EAE模型)
- 模型背景:MOG35-55联合百日咳毒素诱导变态反应性脑脊髓炎(EAE)模型构建方法,是一种常用的研究多发性硬化(MS)及其相关自身免疫性疾病的动物模型构建方法。以下是详细的构建步骤和注意事项。
- 实验准备
- 实验动物:选用对EAE敏感的近交系小鼠,如C57BL/6小鼠。小鼠的年龄和体重应根据实验需求确定,通常选用6-8周龄的雌性小鼠。
- 实验材料:
- MOG35-55多肽:作为诱导EAE的主要抗原,MOG是髓鞘少突胶质细胞糖蛋白的缩写,其35-55位氨基酸序列是诱导EAE的关键片段。
- 完全弗氏佐剂(CFA):用于增强抗原的免疫原性,CFA中含有结核分枝杆菌作为佐剂成分。
- 百日咳毒素(PTX):作为辅助刺激因子,能够增强EAE的诱导效果。
- 磷酸盐缓冲液(PBS):用于溶解MOG35-55多肽和配制其他溶液。
- 实验设备:
- 注射器、针头:用于皮下注射和尾静脉注射。
- 离心管、移液器:用于溶液配制和混匀。
- 冰盒:用于保持溶液的低温状态。
- 实验步骤
- 抗原乳剂的制备:
- 将MOG35-55多肽溶解在PBS中,配制成一定浓度的溶液。
- 将CFA与MOG35-55溶液按1:1的比例混合,用玻璃注射器反复抽打至油包水状态,制成诱导EAE的抗原乳剂。抽打过程中应在冰上进行,以避免溶液过热导致多肽变性。
- 实验动物分组与免疫:
- 将实验小鼠随机分为正常对照组和EAE模型组。
- EAE模型组小鼠在麻醉状态下,于背部两侧皮下注射制备好的MOG35-55抗原乳剂。注射剂量通常为每只小鼠50-100微升,具体剂量应根据小鼠的体重和实验设计确定。
- 在首次免疫后的特定时间点(如48小时后),EAE模型组小鼠还需通过尾静脉注射PTX作为辅助刺激因子。注射剂量通常为每只小鼠100微升,PTX的浓度应根据实验设计确定。
- 行为学观察与评分:
- 从首次免疫后开始,每日观察并记录小鼠的行为变化。
- 采用特定的评分标准(如0-10分制)对小鼠的神经功能进行评分,以评估EAE的严重程度。评分标准通常包括尾部无力、后肢瘫痪、前肢无力等症状的表现程度。
- 抗原乳剂的制备:
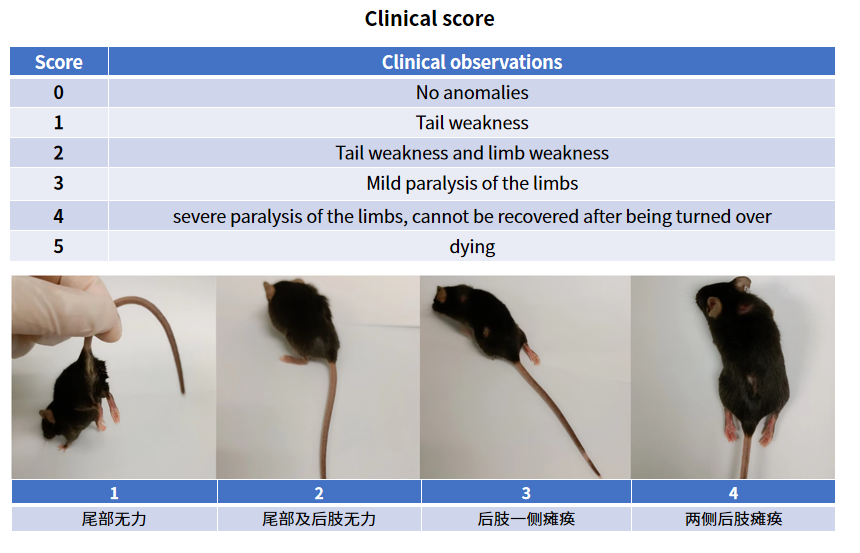
C57BL/6小鼠神经功能评分
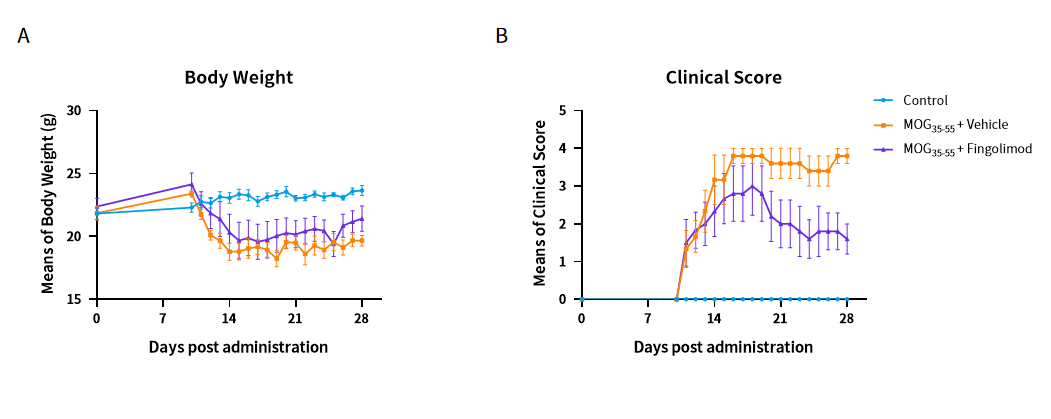
C57BL/6小鼠MOG35-55 EAE 脑模型模型: (A) 体重,(B) 临床评分 (n=5)
- 实验结束与后续处理:
- 在实验结束后,通常观察至小鼠发病高峰后的一段时间(如发病后30天),以评估EAE的病程和恢复情况。
- 处死小鼠后,可取脑和脊髓组织进行病理学检查,以观察炎症细胞浸润、脱髓鞘等病理变化。
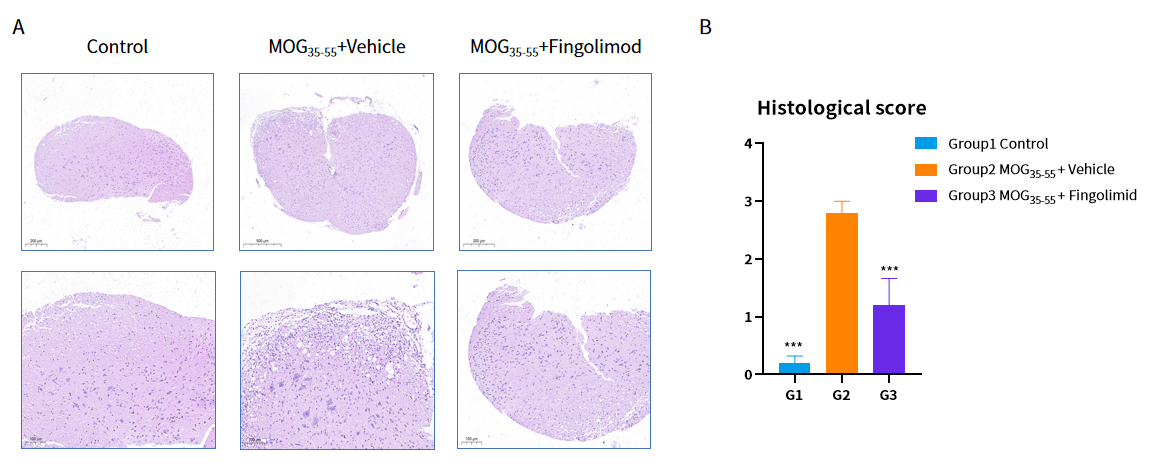
C57BL/6小鼠MOG35-55 EAE 脑模型模型: (A) 病理HE染色,(B) 组织学评分 (n=5)
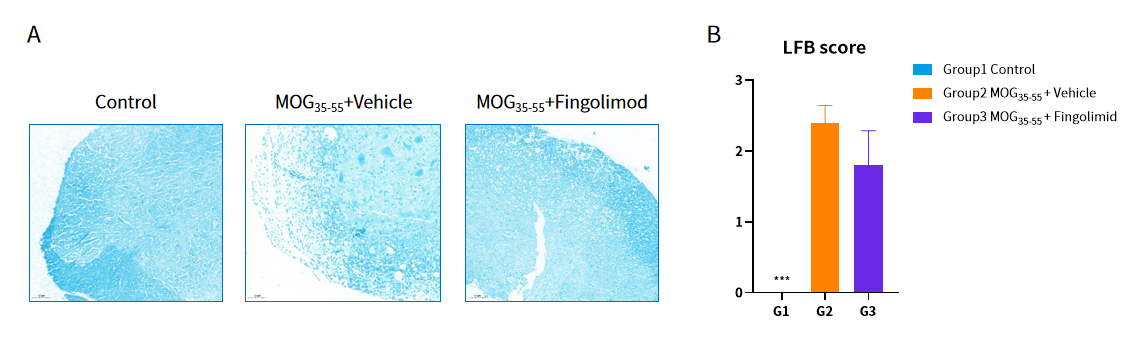
C57BL/6小鼠MOG35-55 EAE 脑模型模型: (A) LFB染色,(B) LFB评分 (n=5)
四、注意事项
-
- 实验动物的选择与饲养:
- 选用对EAE敏感的近交系小鼠,以减少个体差异对实验结果的影响。
- 实验前应确保小鼠饲养环境清洁、安静,以减少外界因素对实验结果的影响。
- 抗原乳剂的制备:
- 确保MOG35-55多肽和CFA充分混合,制备成均匀的抗原乳剂。
- 抗原乳剂的制备应在冰上进行,以避免溶液过热导致多肽变性。
- 注射操作:
- 注射前应麻醉小鼠,以减少其痛苦和挣扎。
- 注射时应准确、缓慢地推进注射器,避免漏液或损伤组织。
- 行为学观察与评分:
- 观察时应保持安静、舒适的环境,避免外界因素对小鼠行为的干扰。
- 评分时应客观、准确,以减少主观误差。
- 实验结束与后续处理:
- 在实验结束后,应及时处死小鼠并进行后续处理,以减少动物痛苦和伦理问题。
- 组织病理学检查时应采用多种方法相结合,以提高诊断的准确性。
- 实验动物的选择与饲养:
五、模型特点与应用
-
- 模型特点:
- MOG35-55联合百日咳毒素诱导的EAE模型具有发病率高、病情严重的特点。
- 该模型能够模拟人类多发性硬化(MS)的部分病理生理特征,如脱髓鞘、炎症细胞浸润等。
- 应用:
- 该模型可用于筛选和评价治疗MS及其相关自身免疫性疾病的药物。
- 通过研究该模型,可以深入了解MS的发病机制,为临床治疗提供理论依据。
- 模型特点:
六、勋博脑膜炎模型未来方向
- 复杂模型构建:
- 类器官-动物嵌合模型:人源化BBB类器官移植小鼠,模拟人类免疫应答
- 基因编辑模型:CRISPR-Cas9敲入人类IL-6基因,提升炎症反应真实性
- 动态监测体系:
- 纳米传感器植入:实时监测脑脊液IL-1β变化
- 多模态影像整合:fMRI+PET量化神经胶质网络损伤
- 行为学观察与评分:
- 从首次免疫后开始,每日观察并记录小鼠的行为变化。
- 采用特定的评分标准(如0-10分制)对小鼠的神经功能进行评分,以评估EAE的严重程度。评分标准通常包括尾部无力、后肢瘫痪、前肢无力等症状的表现程度。
