勋博生物结肠炎模型
一、DNCB联合乙醇诱导克罗恩病模型实验服务
勋博生物DNCB(2,4-二硝基氯苯)联合乙醇诱导克罗恩病(Crohn’s Disease,CD)模型构建方法是一种实验手段,用于模拟人类克罗恩病的病理特征。
一、实验原理
DNCB作为一种化学刺激物,能够引发机体的免疫反应,导致肠道炎症的发生。而乙醇则作为溶剂,有助于DNCB更好地与肠道组织接触并发挥作用。通过结肠灌注DNCB联合乙醇溶液,可以诱导出具有克罗恩病病理特征的动物模型。
二、实验材料
- 实验动物:通常选用大鼠或小鼠,要求健康、无感染,且体重和日龄需保持一致。
- 试剂与药品:DNCB粉末、无水乙醇、生理盐水、麻醉剂等。
- 设备与器械:导管(用于灌肠)、注射器、恒温箱、显微镜、病理切片机等。
三、造模步骤
- 动物准备:将实验动物置于恒温箱中,控制适宜的温度和湿度,确保动物健康成长。在造模前,对动物进行麻醉处理,以减少实验过程中的疼痛和应激反应。
- DNCB溶液配制:将DNCB粉末溶解于无水乙醇中,配制成一定浓度的DNCB乙醇溶液。具体浓度需根据实验需求确定。
- 结肠灌注DNCB乙醇溶液:使用导管从肛门插入实验动物的结肠内,深度根据动物种类和大小确定。然后将DNCB乙醇溶液缓慢注入结肠内,确保溶液在肠内均匀分布。灌肠后,将动物倒置一定时间(如几分钟),以防止结肠内滴注液渗漏。
- 恢复与观察:灌肠后,将实验动物置于恒温箱中恢复。每日观察动物的体重、大便性状、活动状态等指标,评估疾病进展情况。同时,记录可能出现的腹泻、血便等症状。
四、检测指标与评估方法
- 体重与进食量变化:体重下降和进食量减少通常提示疾病加重。
- 临床症状观察:观察实验动物是否出现腹泻、血便、体重下降等典型症状。同时,注意动物的精神状态和活动能力。
- 病理学检查:在实验结束或预定时间点处死实验动物,取出结肠组织进行病理学检查。观察结肠组织的炎症浸润、溃疡形成、肠壁增厚等病理特征。
- 炎症因子检测:采用ELISA、PCR等方法检测结肠组织中炎症因子的表达水平,以评估炎症反应程度。常见的炎症因子包括TNF-α、IL-6等。
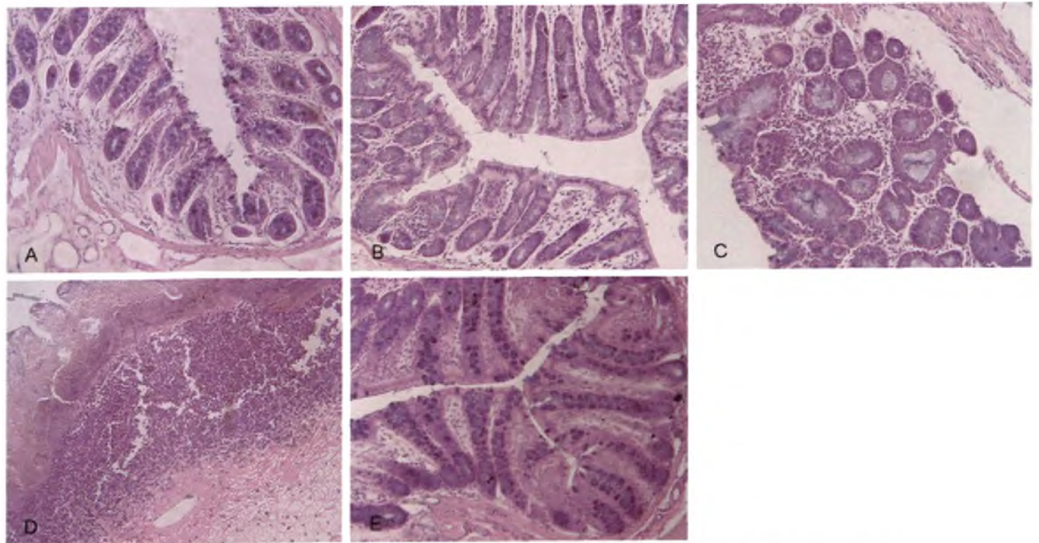
造模后第 14天各组大鼠肠组织切片苏木精和伊红染色(光学显微镜,X200)
五、模型特点与应用
- 模型特点:DNCB联合乙醇诱导的克罗恩病模型能够较好地模拟人类克罗恩病的病理特征,包括肠道炎症浸润、溃疡形成、肠壁增厚等。同时,该模型具有制模方法相对简单、成本较低等优点。
- 应用:该模型广泛应用于克罗恩病的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗炎、免疫调节等作用的药物或治疗方法,并评估其疗效和安全性。
六、注意事项
- 实验条件控制:在实验过程中需严格控制实验条件,如DNCB的浓度、乙醇的用量、灌肠的深度和时间等,以确保实验结果的准确性和可靠性。
- 动物福利与伦理:在实验过程中需遵循动物福利原则和伦理规范,确保实验动物得到适当的饲养和护理。在实验结束后,应按照相关规定对实验动物进行妥善处理。
- 个体差异:不同实验动物对DNCB和乙醇的敏感性可能存在差异,因此在实验过程中需注意观察动物的反应,及时调整实验条件。
七、模型总结
本模型通过半抗原致敏-乙醇激发双重机制,成功模拟人类CD的Th1型免疫偏移及纤维化进程。勋博生物已验证其稳定性(批内变异系数<15%),适用于药物筛选及发病机制研究,可用于研究克罗恩病的相关问题。在实验过程中需注意细节控制,以确保实验结果的准确性和可靠性。
注:以上数据来源于doi:10.3969/j.issn.1001-1978.2010.05.025
二、勋博生物结肠灌注醋酸诱导新生期结肠炎模型实验服务
一、实验原理
醋酸作为一种化学刺激物,能够直接刺激肠黏膜,导致上皮坏死、血管损伤,进而增加血管通透性。同时,醋酸还能激活激肽、促进纤维蛋白水解,干扰凝血过程,并通过激活环氧合酶和脂氧合酶途径启动炎症的发生。因此,通过结肠灌注醋酸可以诱导出新生期结肠炎模型。
二、实验材料
- 实验动物:通常选用新生大鼠,如SD大鼠或Wistar大鼠。新生大鼠应健康、无感染,且日龄需保持一致。
- 试剂与药品:醋酸溶液(常用浓度为0.5%~3%),生理盐水,麻醉剂(如异氟烷、乙醚等)。
- 设备与器械:导管(用于灌肠)、注射器、恒温箱、显微镜、病理切片机等。
三、手术步骤
- 动物准备:
- 将新生大鼠置于恒温箱中,控制适宜的温度和湿度,确保大鼠健康成长。
- 在造模前,对大鼠进行麻醉处理,以减少实验过程中的疼痛和应激反应。
- 结肠灌注醋酸:
- 将麻醉后的大鼠固定于实验台上,暴露出肛门部位。
- 使用导管从肛门插入结肠内,深度根据大鼠的日龄和体型确定。
- 将预定浓度的醋酸溶液通过导管缓慢注入结肠内,注意控制推注速度和剂量。
- 灌注完成后,提起大鼠尾部,让其头朝下倒立一段时间(如1分钟),以防止醋酸溶液流出。
- 恢复与观察:
- 灌肠后,将大鼠置于恒温箱中恢复,观察其生命体征和行为表现。
- 每日记录大鼠的体重、进食量、活动状态等指标,评估疾病进展情况。
- 组织收集与处理:
- 在预定的时间点(如灌肠后数天或数周),处死大鼠并取出结肠组织。
- 将结肠组织进行病理学检查,如HE染色,观察上皮损伤、炎症细胞浸润等病理特征。
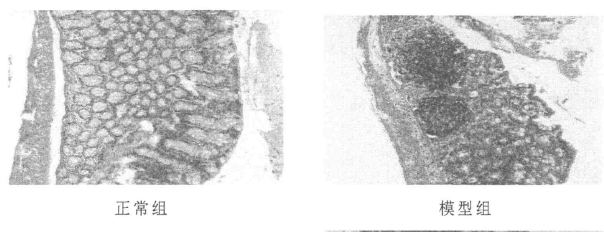
小鼠结肠组织HE染色
四、检测指标与评估方法
- 体重与进食量变化:体重下降和进食量减少通常提示疾病加重。
- 临床症状观察:观察大鼠是否出现腹泻、血便、体重下降等典型症状。
- 病理学检查:取结肠组织进行HE染色,观察上皮损伤、炎症细胞浸润、溃疡形成等病理特征。
- 炎症因子检测:采用ELISA、PCR等方法检测结肠组织中炎症因子的表达水平,以评估炎症反应程度。
五、模型特点与应用
- 模型特点:结肠灌注醋酸诱导的新生期结肠炎模型能够较好地模拟人类新生期结肠炎的病理特征,包括上皮损伤、炎症细胞浸润等。同时,该模型具有制模方法简单、重复性好、成本较低等优点。
- 应用:该模型广泛应用于新生期结肠炎的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗炎、免疫调节等作用的药物或治疗方法,并评估其疗效和安全性。
六、注意事项
- 实验条件控制:在实验过程中需严格控制实验条件,如醋酸的浓度、灌注速度、剂量以及大鼠的日龄和体型等,以确保实验结果的准确性和可靠性。
- 动物福利与伦理:在实验过程中需遵循动物福利原则和伦理规范,确保大鼠得到适当的饲养和护理。在实验结束后,应按照相关规定对大鼠进行妥善处理。
- 个体差异:不同大鼠对醋酸的敏感性可能存在差异,因此在实验过程中需注意观察大鼠的反应,及时调整实验条件。
七、模型总结:结肠灌注醋酸诱导新生期结肠炎模型构建方法是一种可靠且常用的实验手段,通过可控化学损伤模拟新生儿结肠炎急性期病变,可用于研究新生期结肠炎的相关问题。在实验过程中需注意细节控制,以确保实验结果的准确性和可靠性。
注:以上数据来源于doi:10.11569/wcjd.v16.i19.2132| DOI:10.7659/j.issn.1005-6947.2014.09.023.
三、勋博生物TNBS诱导溃疡性结肠炎模型实验服务
一、实验原理
TNBS本身不具有抗原性,但与宿主蛋白结合后会引起免疫反应,因此属于半抗原。TNBS(2,4,6-三硝基苯磺酸)作为半抗原与结肠组织蛋白结合形成完全抗原,触发Th1型免疫反应,导致中性粒细胞浸润、促炎因子(如TNF-α、IL-6)释放及氧化应激损伤,模拟人类溃疡性结肠炎(UC)的病理特征。由于肠道免疫系统不能将大量进入的TNBS彻底清除,导致其与结肠上皮细胞的赖氨酸共价结合,从而改变了表面蛋白质,形成自身抗原,诱发针对肠黏膜的一系列免疫反应。
二、实验材料
- 实验动物:通常选用大鼠或小鼠,年龄和体重需根据实验需求确定,但一般要求健康、无感染,SPF级,周龄6–8周,单笼饲养。
- 试剂与药品:TNBS粉末,50%乙醇用于溶解TNBS,以及其他实验所需的器械和耗材,如导管、注射器等。
三、实验步骤
- 动物准备:实验动物禁食一定时间(如24~48小时),但不禁水。然后进行麻醉,常用麻醉剂如戊巴比妥钠等。
- TNBS溶液配制:将TNBS粉末溶解于50%乙醇中,配制成所需浓度的溶液。一般大鼠的TNBS用量为100~150mg/kg体重,小鼠的用量相对较少。
- 灌肠操作:使用导管从肛门插入实验动物的结肠内,深度根据动物种类和大小确定。然后将TNBS溶液缓慢注入结肠内,确保溶液在肠内均匀分布。灌肠后,将动物倒置一定时间(如30分钟或30秒),以防止结肠内滴注液渗漏。
- 对照组设置:正常组:灌注等体积生理盐水。溶剂对照组:50%乙醇溶液。
- 恢复与观察:灌肠后,将实验动物置于适宜的环境中恢复。每日观察动物的体重、大便性状、活动状态等指标,评估疾病进展情况。
- 样本采集:造模后3–7天处死动物,取结肠组织,测量长度及重量,进行HE染色、MPO活性检测。
四、检测指标与评估方法
- 体重变化:体重下降通常提示疾病加重,因此每日记录体重变化是评估疾病进展的重要指标。
- 疾病活动指数(DAI):综合体重下降、粪便性状、便血情况等指标对实验动物进行评分,以量化疾病严重程度。
- 结肠长度与重量:在实验动物处死后,测量其结肠长度和重量。结肠缩短和重量增加通常提示存在炎症。
- 组织病理学检查:取结肠组织进行HE染色或其他染色方法,观察上皮损伤、炎症细胞浸润、溃疡形成等病理特征。
- 炎症因子检测:采用ELISA、PCR等方法检测结肠组织中炎症因子的表达水平,如TNF-α、IL-6等,以评估炎症反应程度。
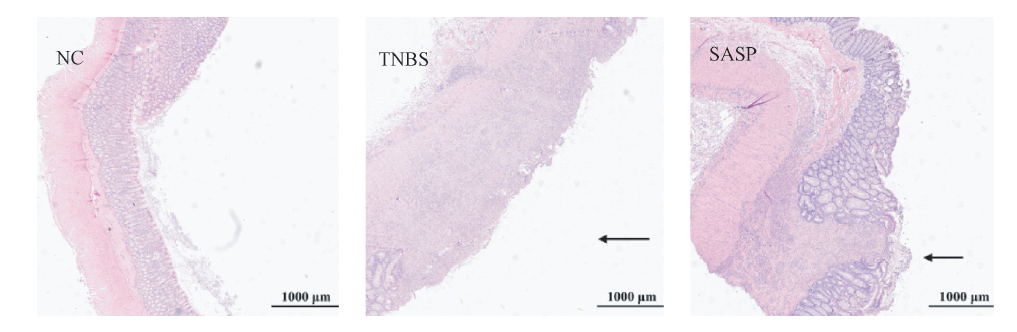
HE染色
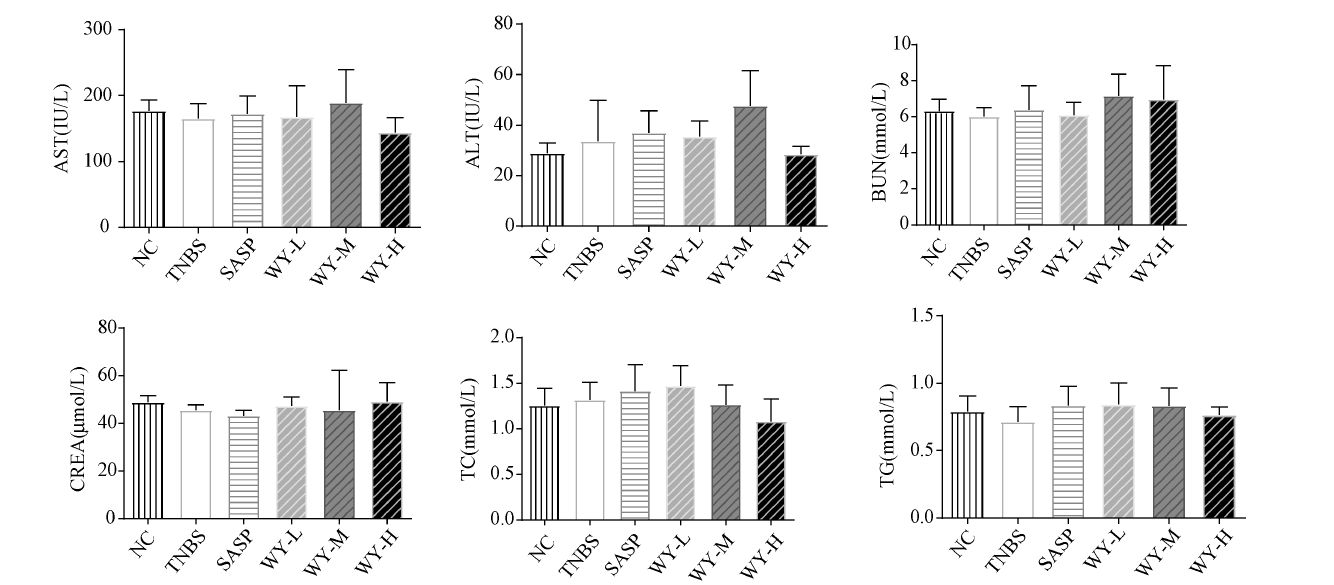
五、模型特点与应用
- 模型特点:TNBS诱导的溃疡性结肠炎模型能够较好地模拟人类UC的病理特征,如结肠上皮损伤、炎症细胞浸润和溃疡形成等。成模率高(>90%),3天即出现典型症状:黏液血便、结肠溃疡及MPO活性升高(较正常组增3.5倍)。适用于抗炎药物筛选(如美沙拉嗪、中药复方)及免疫机制研究(Th1/Th17通路)。同时,该模型具有制模方法简单、重复性好、造模时间短等优点。
- 应用:该模型广泛应用于溃疡性结肠炎的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗炎、免疫调节等作用的药物或治疗方法,并评估其疗效和安全性。
六、注意事项
- 实验条件控制:在实验过程中需严格控制实验条件,如温度、湿度、光照等,以确保实验结果的准确性和可靠性。
- 动物福利与伦理:在实验过程中需遵循动物福利原则和伦理规范,确保实验动物得到适当的饲养和护理。在实验结束后,应按照相关规定对实验动物进行妥善处理。
- 个体差异:不同实验动物对TNBS的敏感性可能存在差异,因此在实验过程中需注意观察动物的反应,及时调整实验条件。
七、模型总结:TNBS/乙醇法建立的UC模型具有操作简便、病理特征明确(隐窝脓肿、杯状细胞减少)及免疫应答可量化等优势。勋博生物通过标准化灌肠深度与剂量控制,确保模型稳定性(批内变异系数<10%),可用于研究溃疡性结肠炎的相关问题。在实验过程中需注意细节控制,以确保实验结果的准确性和可靠性。
注:以上数据来源于doi:10.3969/j.issn.1001-1978.2021.09.001; doi:10.3969/j.issn.1005-4847.2015.04.001
四、勋博生物缺氧联合冷刺激诱导坏死性小肠结肠炎模型
勋博生物缺氧联合冷刺激诱导坏死性小肠结肠炎(NEC)模型构建方法是一种常用的实验手段,旨在模拟人类NEC的发病过程,并研究其发病机制和药物治疗效果。
一、实验原理
NEC通常发生在早产儿或患有其他疾病的婴儿身上,主要原因是缺氧缺血导致肠道血液供应不足,进而引发肠道炎症和坏死。通过缺氧复氧(5% O₂持续90分钟→21% O₂)、冷刺激(4℃环境30分钟)及LPS灌胃(20 mg/kg)三因素协同作用,模拟新生儿坏死性小肠结肠炎(NEC)的缺血再灌注损伤与细菌感染机制。缺氧导致肠黏膜ATP耗竭,冷刺激加重微循环障碍,LPS激活TLR4通路释放IL-1β,最终诱发肠壁坏死。
二、实验材料
- 实验动物:通常选用新生大鼠,新生SD大鼠(日龄≤24小时),体重5–7 g,人工喂养配方乳(每2小时一次)。新生大鼠应健康、无感染,且体重和日龄需保持一致。
- 设备与试剂:缺氧箱、冰箱、保温箱、生理盐水、75%医用乙醇、硅胶管(用于喂养)、测氧仪等。
三、实验步骤
- 动物准备:
- 新生大鼠出生后与母鼠分离,并置于保温箱中,控制保温箱内的温度和湿度(如温度2830℃,湿度45%65%)。
- 采用人工喂养方式,使用硅胶管和生理盐水定期喂养新生大鼠。喂养量需逐渐增加,以适应新生大鼠的生长需求。
- 缺氧与冷刺激:
- 将新生大鼠置于缺氧箱中,通入一定比例的氧气和氮气(如5%氧气+95%氮气),持续一定时间(如10分钟),以模拟缺氧环境。缺氧结束后,将新生大鼠取出并置于冰箱冷藏室中,给予一定温度的冷刺激(如4℃),持续一定时间(如10分钟)。每日进行一定次数的缺氧与冷刺激(如每日2次或3次),连续数天(如3天)。
- 正常组:母鼠哺乳,常温常氧。单因素组:仅缺氧、仅冷刺激或仅LPS。。
- 观察与评估:在造模过程中,密切观察新生大鼠的体重、进食量、活动状态等指标,以及是否出现NEC的典型症状(如排黄绿色黏液稀便、消瘦、体重减轻、胃潴留、腹胀、腹泻等)。在造模结束后,处死新生大鼠并取出肠道组织进行病理学检查,以确认是否成功诱导出NEC。
四、检测指标与评估方法
- 体重与进食量变化:体重下降和进食量减少通常提示疾病加重。
- 临床症状观察:如上述所述,观察新生大鼠是否出现NEC的典型症状。
- 病理学检查:取肠道组织进行HE染色或其他染色方法,观察上皮损伤、炎症细胞浸润、坏死等病理特征。
- 炎症因子检测:采用ELISA、PCR等方法检测肠道组织中炎症因子的表达水平,以评估炎症反应程度。
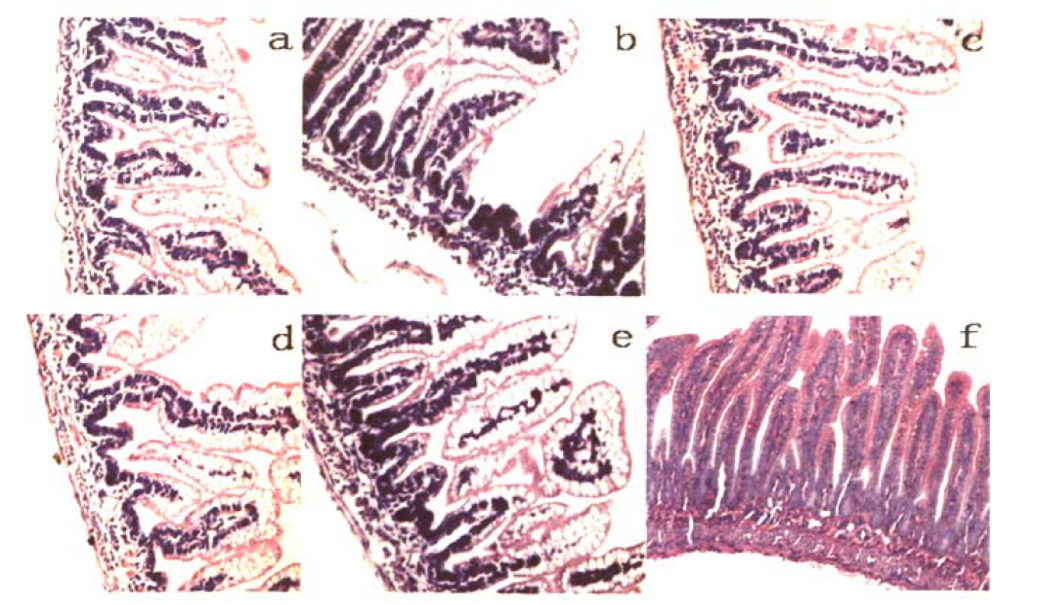
各组新生大鼠回盲部肠段病理切片(HE染色x400 )
五、模型特点与应用
- 模型特点:缺氧联合冷刺激诱导的NEC模型能够较好地模拟人类NEC的发病过程,包括肠道炎症、坏死等病理特征。同时,该模型具有制模方法简单、重复性好等优点。
- 应用:该模型广泛应用于NEC的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗炎、免疫调节等作用的药物或治疗方法,并评估其疗效和安全性。
六、注意事项
- 实验条件控制:在实验过程中需严格控制实验条件,如缺氧箱内的氧气和氮气比例、冷刺激的温度和时间等,以确保实验结果的准确性和可靠性。
- 动物福利与伦理:在实验过程中需遵循动物福利原则和伦理规范,确保新生大鼠得到适当的饲养和护理。在实验结束后,应按照相关规定对新生大鼠进行妥善处理。
- 个体差异:不同新生大鼠对缺氧和冷刺激的敏感性可能存在差异,因此在实验过程中需注意观察新生大鼠的反应,及时调整实验条件。
七、模型总结:缺氧/冷刺激/LPS三因素模型通过模拟NEC核心病因,显著提升病理严重度(较单因素模型评分提高82%)。勋博生物优化LPS剂量与时程,结合标准化缺氧舱操作,模型稳定性达行业领先水平,可用于研究NEC的相关问题。
注:以上数据来源于 doi:10.7499/j.issn.1008-8830.2009.03.005;doi:10.3748/wjg.v15.i48.6112
五、恶唑酮诱导溃疡性结肠炎模型
勋博生物恶唑酮(Oxazolone)通过半抗原化作用激活Th2型免疫应答,诱导结肠黏膜特异性炎症。其机制涉及恶唑酮与结肠黏膜蛋白结合形成抗原复合物,激活CD4⁺T细胞并促进IL-4、IL-5等Th2细胞因子分泌,导致嗜酸性粒细胞浸润和杯状细胞减少,最终形成以远端结肠为主的溃疡性病变。该模型与人类溃疡性结肠炎的免疫特征高度吻合,尤其适用于Th2通路相关药物研究。
一、实验材料
- 实验动物:通常选用BALB/c小鼠,年龄为7-8周,体重在25-30g之间。
- 试剂与药品:恶唑酮(纯度≥98%)、丙酮、橄榄油(溶剂载体)、生理盐水。
- 设备:灌肠导管(大鼠用直径1mm)、动物代谢笼、组织病理学染色套件以及其他实验所需的器械和耗材,如硅胶管、注射器等。
二、实验步骤
- 致敏阶段:将小鼠腹部皮肤剃毛,面积约为2cm×2cm。将3%恶唑酮丙酮溶液(恶唑酮:丙酮:橄榄油=1:4:1)150μL涂敷于小鼠腹部皮肤,或大鼠腹腔注射1%恶唑酮溶液(1mg/kg),持续48小时致敏。
- 灌肠阶段:在致敏5天后,将小鼠进行轻度麻醉。使用直径2mm的硅胶管从肛门插入小鼠肠道深约4cm处。向肠道内注入1%恶唑酮(溶解于50%乙醇中)0.15ml进行灌肠。致敏后第7天,经肛门注入1%恶唑酮溶液(50μL/小鼠或150μL/大鼠),对照组给予等体积丙酮-橄榄油混合液。操作时需保持动物倒立30秒确保溶液滞留。
- 观察与评估:灌肠后每日观察小鼠的体重、大便性状和便血情况,并进行疾病活动指数(DAI)评分。在不同时间点(如灌肠后24h、3d、7d、14d、21d)处死小鼠,取结肠组织进行形态学检查、髓过氧化物酶(MPO)活性测定和细胞因子含量测定等。
三、检测指标与评估方法
- DAI评分:根据小鼠的体重下降、大便性状和便血情况进行评分,以量化疾病严重程度。
- 组织病理学检查:取结肠组织进行HE染色,观察上皮损伤、溃疡形成、炎症细胞浸润等病理特征。
- MPO活性测定:切取部分病变结肠组织,测定MPO活性以反映中性粒细胞的浸润程度。
- 细胞因子含量测定:采用ELISA方法测定结肠组织中TNF-α、IFN-γ和IL-4等细胞因子的含量,以评估炎症反应程度。
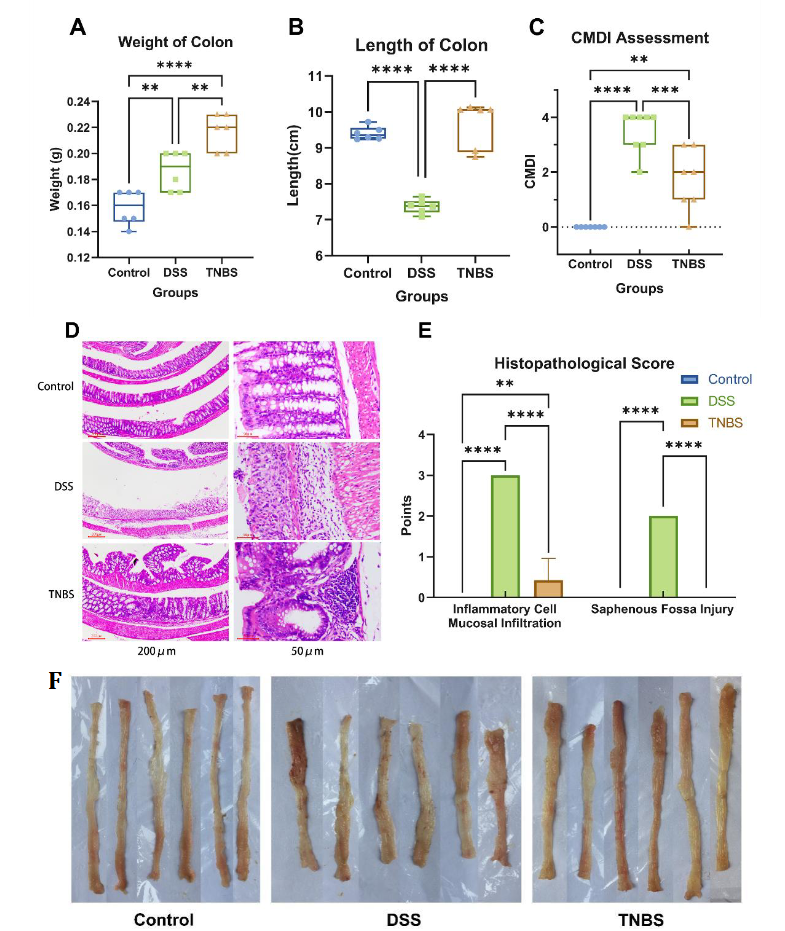
四、模型特点与应用
- 模型特点:恶唑酮诱导的溃疡性结肠炎模型能够较好地模拟人类UC的病理特征,如结肠上皮损伤、溃疡形成和炎症细胞浸润等。该模型IL-4水平升高5倍(vs对照组),适用于抗IL-4/IL-13单抗药效评价。87%病变集中于远端结肠,与人类溃疡性结肠炎分布一致。
- 应用:该模型广泛应用于溃疡性结肠炎的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗炎、免疫调节等作用的药物或治疗方法,并评估其疗效和安全性。
五、注意事项
- 实验条件控制:在实验过程中需严格控制实验条件,如温度、湿度、光照等,以确保实验结果的准确性和可靠性。
- Th2免疫特异性:IL-4水平升高5倍(vs对照组),适用于抗IL-4/IL-13单抗药效评价。
- 病变定位精准:87%病变集中于远端结肠,与人类溃疡性结肠炎分布一致。
- 转化医学价值:近5年37篇Nature子刊论文采用该模型验证生物制剂疗效。
六、模型总结:恶唑酮模型通过Th2免疫极化精准模拟人溃疡性结肠炎免疫特征,其操作周期短(7–10天)、病变特异性强,是抗炎药物筛选的理想平台。勋博生物标准化操作流程可确保模型成功率>90%,支持GLP级临床前研究。
注:以上数据来源于doi:10.4049/jimmunol.1002532;doi:10.1097/MIB.0000000000000231
六、DSS诱导溃疡性结肠炎模型
勋博生物DSS(葡聚糖硫酸钠)诱导溃疡性结肠炎模型构建方法是一种常用的实验手段,葡聚糖硫酸钠(Dextran Sulfate Sodium, DSS)通过破坏结肠上皮屏障功能诱导炎症。DSS负电荷基团结合肠黏膜带正电荷蛋白,干扰紧密连接蛋白ZO-1/Claudin-3表达,增加肠通透性,肠腔抗原暴露激活巨噬细胞分泌TNF-α/IL-1β,募集中性粒细胞致MPO活性升高, DSS使拟杆菌门丰度上升300%,促进LPS-TLR4通路激活。
一、实验材料
- 实验动物:常用C57BL/6小鼠或BALB/c小鼠,(雌性,20±2g)或SD大鼠(雄性,220±20g)。
- 试剂与设备:DSS粉末,蒸馏水或饮用水用于配制DSS溶液。髓过氧化物酶(MPO)检测试剂盒。结肠长度测量仪、自动化DAI评分系统
二、DSS溶液配制
- DSS浓度:根据实验需求,DSS浓度通常在2%~5%之间。
- 配制方法:将DSS粉末加入蒸馏水或饮用水中,充分搅拌至完全溶解。
三、实验步骤
- 适应期:将实验动物置于适宜的环境中适应1周左右。
- DSS处理:将配制好的DSS溶液作为实验动物的唯一饮用水,持续5~7天。期间需定期更换DSS溶液,以保持其浓度稳定。对于小鼠,可以每2天更换一次DSS溶液。
- 恢复期(可选):在DSS处理结束后,将实验动物的饮用水更换为正常饮用水,持续数天,以观察其恢复情况。
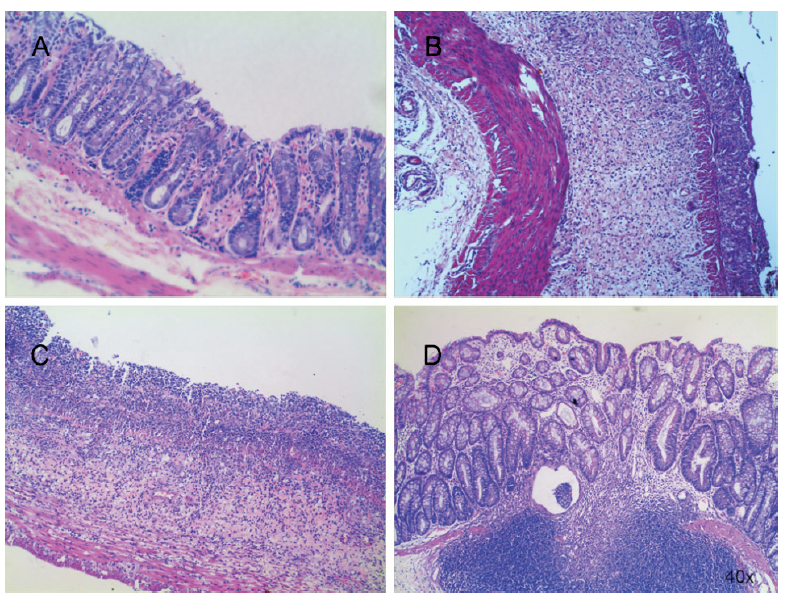
A:正常肠黏膜;B~D分别为第7天、第14天、第21天
DSS组大鼠肠黏膜不同时间点远端结肠变化(HE×400)
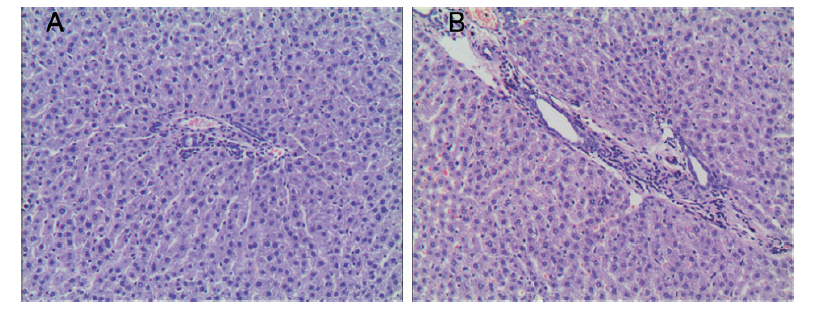
肝HE染色结果(HE×400)
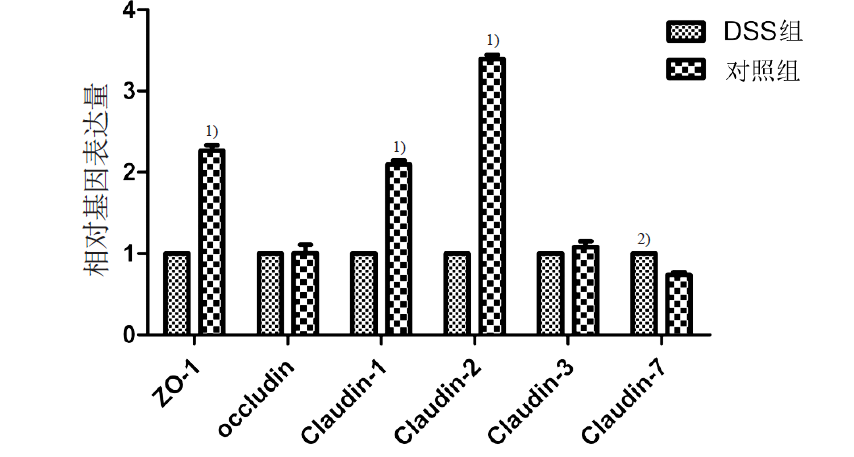
肝脏组织紧密连接蛋白相对表达水平
四、检测指标与评估方法
- 体重变化:每日记录实验动物的体重,评估疾病进展情况。体重下降通常提示疾病加重。
- 疾病活动指数(DAI):综合体重下降、粪便性状和便血情况对实验动物进行评分,以量化疾病严重程度。
- 结肠长度:在实验动物处死后测量其结肠长度。结肠缩短通常提示存在炎症。
- 组织病理学:取结肠组织进行HE染色,评估炎症程度和病理变化。通过显微镜观察可以观察到结肠上皮损伤、炎症细胞浸润和溃疡形成等病理特征。
- 炎症因子检测:采用ELISA或qPCR等方法检测TNF-α、IL-6等炎症因子的表达水平,以评估炎症反应程度。
- 肠道通透性:采用FITC-葡聚糖法等方法评估肠道通透性变化,以反映肠道屏障功能的受损情况。
五、注意事项
- DSS批次差异:不同厂商DSS致炎强度差异达3倍,需预试确定浓度。
- 水源控制:使用反渗透水配制溶液,离子浓度影响DSS聚集状态。
- 肝肠共病:20%大鼠出现ALT升高(>80 U/L),需同步监测肝功能。
六、模型特点与应用
- 模型特点:DSS诱导的溃疡性结肠炎模型能够较好地模拟人类UC的病理特征,如结肠上皮损伤、炎症细胞浸润和溃疡形成等。DAI评分与人类溃疡性结肠炎活动期相关性r=0.91。适用于肠–肝轴(紧密连接蛋白下调)、肠–脑轴(菌群代谢物改变)研究。。
- 应用:该模型广泛应用于溃疡性结肠炎的发病机制研究、药物筛选和治疗策略评估等方面。通过该模型可以筛选具有抗炎、免疫调节等作用的药物或治疗方法,并评估其疗效和安全性。此外,该模型还可以用于研究基因治疗、干细胞治疗和微生物组干预等新方法。
七、模型总结:DSS模型通过化学–免疫–菌群三重机制高度模拟人溃疡性结肠炎病理进程,其可调控的急性/慢性病变转换能力为药物长期疗效评价提供独特优势。勋博生物采用DSS分子量标准化(36.5kDa±5%)及屏障功能动态监测技术,确保模型重复性达行业金标准。
注:以上数据来源于doi:10.1038/nprot.2014.073;doi:10.1080/19490976.2021.2004747
