调理作用诱导巨噬细胞吞噬无载体胆红素/JPH203纳米粒子以抑制炎症从而治疗骨关节炎
- 27 5 月, 2025
- 12:38 下午
Huirong Huang.et al:
Opsonization Inveigles Macrophages Engulfing Carrier‐Free Bilirubin/JPH203 Nanoparticles to Suppress Inflammation for Osteoarthritis Therapy
Advanced Science 2024年
影响因子/JCR分区:14.3/Q1
中文标题:调理作用诱导巨噬细胞吞噬无载体胆红素/JPH203纳米粒子以抑制炎症从而治疗骨关节炎
运用技术:活体成像,Micro CT扫描,代谢组学技术,免疫组化,免疫荧光,HE等病理染色,巨噬细胞培养等

IgG/BRJ的制备
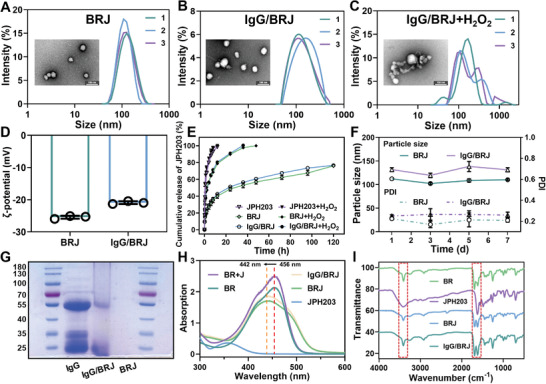
纳米颗粒 IgG/BRJ 的表征
A) BRJ
B) IgG/BRJ
C) IgG/BRJ 在 H 2 O 2存在下的粒度分布和 TEM 图像。
D) BRJ 和 IgG/BRJ 的 Zeta 电位。
E) 在含有 0.5% Tween 80(含或不含 0.3% H 2 O 2)的磷酸盐缓冲溶液(PBS;pH 7.4)中,JPH203 从游离 JPH203、BRJ 和 IgG/BRJ 中体外释放的概况。
F ) 通过测定 7 天内的粒度和 PDI 研究 BRJ 和 IgG/BRJ 的稳定性。
G) SDS-PAGE 凝胶中 IgG、IgG/BRJ 和 BRJ 的考马斯亮蓝染色图像。
H)BR、JPH203、BR与JPH203混合物、BRJ与IgG/BRJ的紫外可见光谱。
I)BR、JPH203、BRJ和IgG/BRJ的傅里叶变换红外光谱。

IgG/BRJ 促进巨噬细胞 M1 向 M2 极化
M1 巨噬细胞通过产生过多的炎症细胞因子和介质,在促进炎症微环境和 OA 进展中起着关键作用。相反,M2 巨噬细胞表现出抗炎特性,可以阻碍 OA 进展。因此,促进 M1 巨噬细胞复极化为 M2 巨噬细胞代表了一种有前景的 OA 治疗策略。
首先使用免疫荧光 (IF) 分析评估了 IgG/BRJ 体外诱导巨噬细胞从 M1 极化为 M2 表型的潜力,以 CD86 和 Arg-1 分别作为 M1 和 M2 的生物标志物。在 LPS 刺激后观察到 CD86 荧光强度显著增加,同时 Arg-1 荧光强度略有增强(图 3A)。单独使用 BR 或 JPH203 治疗仅产生微小效果。然而,在 BR 和 JPH203 联合治疗组和 IgG/BRJ 组中,CD86 荧光强度明显减弱,而 Arg-1 荧光强度明显增强。值得注意的是,BRJ 的 M2 极化效应弱于 IgG/BRJ,与 BR 和 JPH203 组中观察到的效果相似。BRJ 的摄取低于 IgG/BRJ,导致功能较弱,而游离 BR 和 JPH203 的组合可以直接与细胞相互作用,显示出比 BRJ 更强的作用。这些结果通过定量得到了验证(图 B、C)。
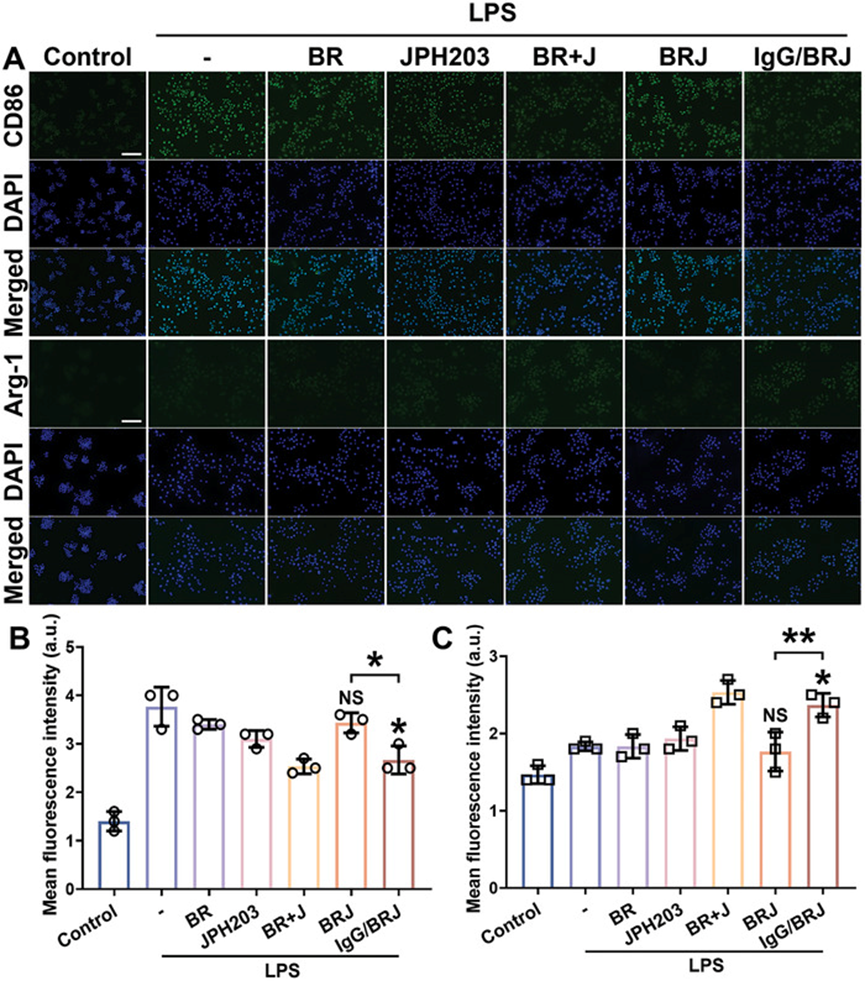
IgG/BRJ 促进巨噬细胞 M1 向 M2 极化
A) 不同处理后,用免疫荧光法检测 M1 生物标志物 CD86 和 M2 生物标志物 Arg-1 的表达,并用 DAPI 标记核位置。比例尺 = 100 µm。
B) 定量分析 CD86 表达的荧光强度。
C) 定量分析 Arg-1 表达的荧光强度。

IgG/BRJ 介导的 M1 至 M2 复极化机制
鉴于 IgG/BRJ 能够诱导 M1-M2 极化,下面实验进一步描述了潜在的调控机制。
- ROS 水平升高是 OA 的主要病理特征。ROS 可促进 M1 巨噬细胞极化,从而加剧滑膜炎、细胞外基质 (ECM) 降解和软骨下骨功能障碍。
- 此外,mTOR 和 NF-κB 信号通路在调节 M1 细胞极化中起着至关重要的作用。由于调理纳米颗粒 IgG/BRJ 主要包含内源性抗氧化剂 BR 和 mTOR 通路抑制剂 JPH203,推测 IgG/BRJ 通过有效清除 ROS 和抑制 mTOR 和 NF-κB 通路来促进 M1-M2 极化。
- 为了评估 ROS 水平,使用 DCFH-DA 荧光探针观察到 LPS 刺激后巨噬细胞中出现强绿色 DCF 信号,这表明 M1 巨噬细胞中的 ROS 水平大幅升高。
- 在治疗组中,BR 和 BR+J 表现出最强的 ROS 消除效果,而 JPH203 也表现出一定的抑制能力。有趣的是,IgG/BRJ 治疗后的 ROS 荧光明显弱于 BRJ 治疗组,表明 IgG/BRJ 制剂具有卓越的 ROS 清除能力。ROS 水平的定量分析进一步证实了这些观察结果(图A、B)。
- 使用蛋白质印迹 (WB) 分析评估 M1 巨噬细胞中 mTOR 和 NF-κB 信号通路成分的表达水平。与对照组相比,M1 巨噬细胞中 p-mTOR、p-NF-κB P65 和 p-IκBα 的表达显着升高,表明通路被激活。然而,经IgG/BRJ处理后,M1巨噬细胞中p-mTOR、p-NF-κB P65和p-IκBα的表达水平显著降低(4C-F)。
- WB结果的定量分析与ROS测量中观察到的趋势一致,表明IgG/BRJ能够通过ROS清除和抑制mTOR和NF-κB信号通路来调节M1-M2巨噬细胞的极化。
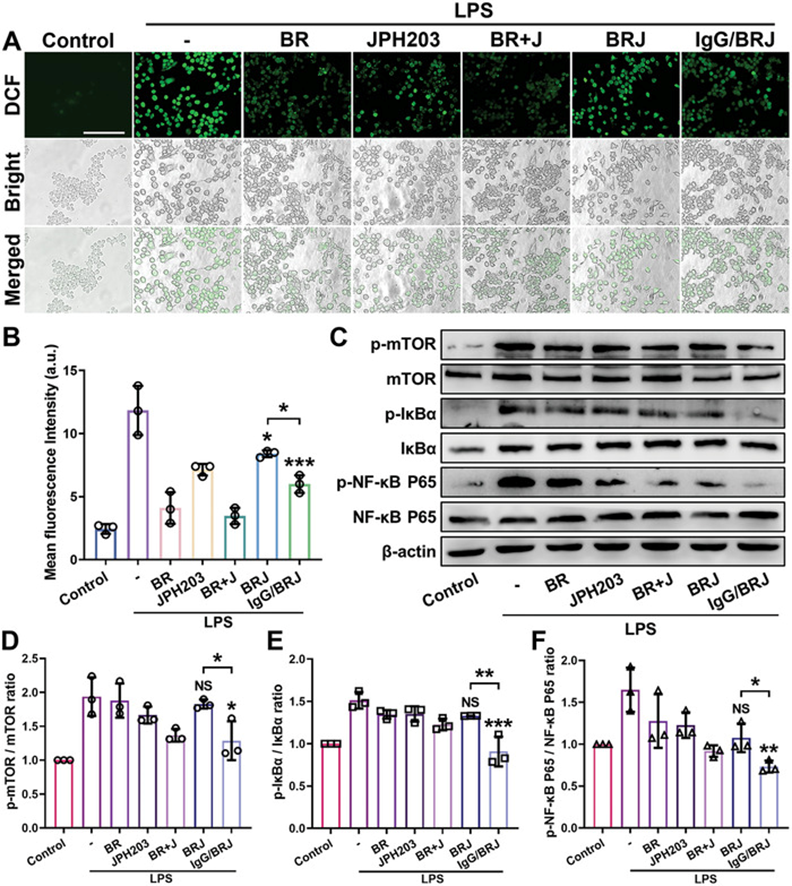
IgG/BRJ 调节巨噬细胞极化的机制
A) 不同处理后,用免疫荧光法检测 M1 生物标志物 CD86 和 M2 生物标志物 Arg-1 的表达,并用 DAPI 标记核位置。比例尺 = 100 µm。
B) 定量分析 CD86 表达的荧光强度。
C) 定量分析 Arg-1 表达的荧光强度。

论证IgG/BRJ对细胞体外代谢调控作用
如前所述,IgG/BRJ 可以通过抑制 mTOR 和 NF-κB 通路以及清除 ROS 来调节 M1‐M2 巨噬细胞极化。鉴于 mTOR 通路与生物体代谢活动之间的密切联系,进行了代谢组学分析以确定 IgG/BRJ 是否通过影响巨噬细胞代谢来影响巨噬细胞极化。
- 分析鉴定了巨噬细胞样本中的 1315 种代谢物,其中与 M1 组相比,IgG/BRJ 处理 (NP) 组中 212 种代谢物显著增加,202 种代谢物显著减少(图A )。
- 维恩图显示 IgG/BRJ 处理和未处理的M1 组之间有 768 种共同的代谢物,其中 26 种和 4 种分别特定于 NP 组和 M1 组(图B)。
- 主成分分析 (PCA) 表明对照组、M1 组和 NP 组的坐标明显分离,表明这三组之间存在显著差异,并强调 IgG/BRJ 治疗对巨噬细胞代谢有显著影响 (图C )。具有相似表达模式的代谢物被认为具有功能意义。
- 因此,对对照组、M1 组和 NP 组的代谢物进行代谢物聚类分析 (图D ),结果与 PCA 中观察到的结果相似。这进一步强调了 IgG/BRJ 治疗组与对照组和 M1 组相比巨噬细胞代谢存在显著差异。
- 随后,使用京都基因与基因组百科全书 (KEGG) 富集和功能途径分析来鉴定突出的能量代谢、炎症调节和生物合成途径 (图E,F )。
- 变量重要性投影 (VIP) 值分析表明,柠檬酸对 IgG/BRJ 诱导的巨噬细胞代谢功能改变有显著贡献(图G)。三羧酸循环(TCA 循环)的激活可以减弱 M1 巨噬细胞的促炎作用,这表明 IgG/BRJ 可能刺激 TCA 循环并促进巨噬细胞向 M2 表型极化。
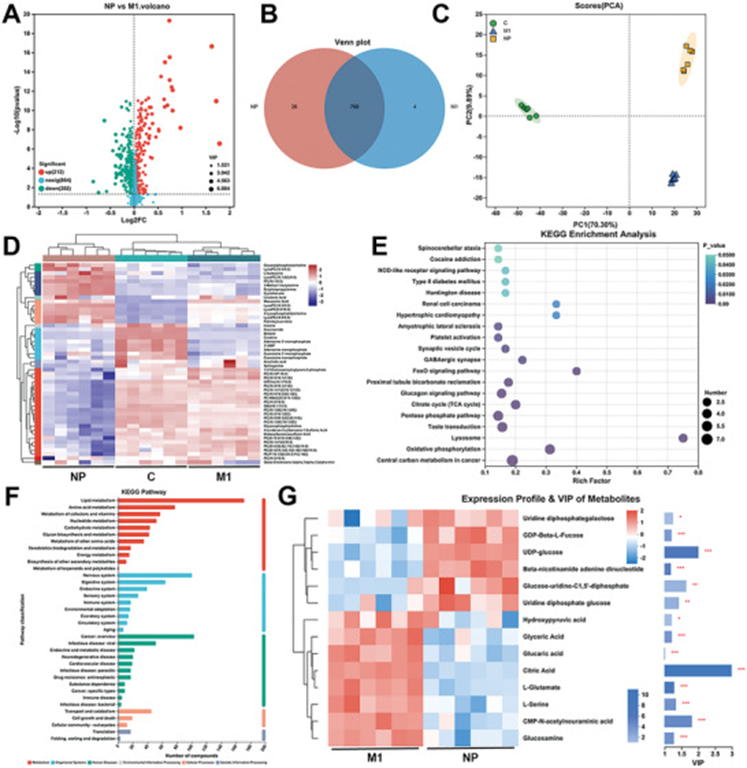
IgG/BRJ对RAW 264.7细胞体外代谢调控作用
A)对照组和LPS处理组RAW 264.7中差异表达代谢物的火山图。红点和绿点分别表示显著上调或下调的代谢物。
B)对照组、M1组和IgG/BRJ处理组(NP组)在RAW 264.7中代谢物表达的Venn图。
C)对照组、M1组和IgG/BRJ处理组(NP组)在RAW 264.7中的二维主成分分析(PCA)得分图。
D)对照组、M1组和IgG/BRJ处理组(NP组)在RAW 264.7中的代谢物聚类分析。E)KEGG通路富集分析,P < 0.05。
F)KEGG功能通路分析。
G) M1 组和 IgG/BRJ 治疗组 (NP) 之间 RAW 264.7 中的 VIP 分析。

论证IgG/BRJ对软骨细胞(RCC)的体外保护作用
M1 巨噬细胞驱动的炎症环境会扰乱软骨细胞代谢,导致分解代谢过程加剧。这会加剧炎症反应并加速 OA 进展。因此,提高软骨细胞的合成代谢水平对于 OA 治疗至关重要。
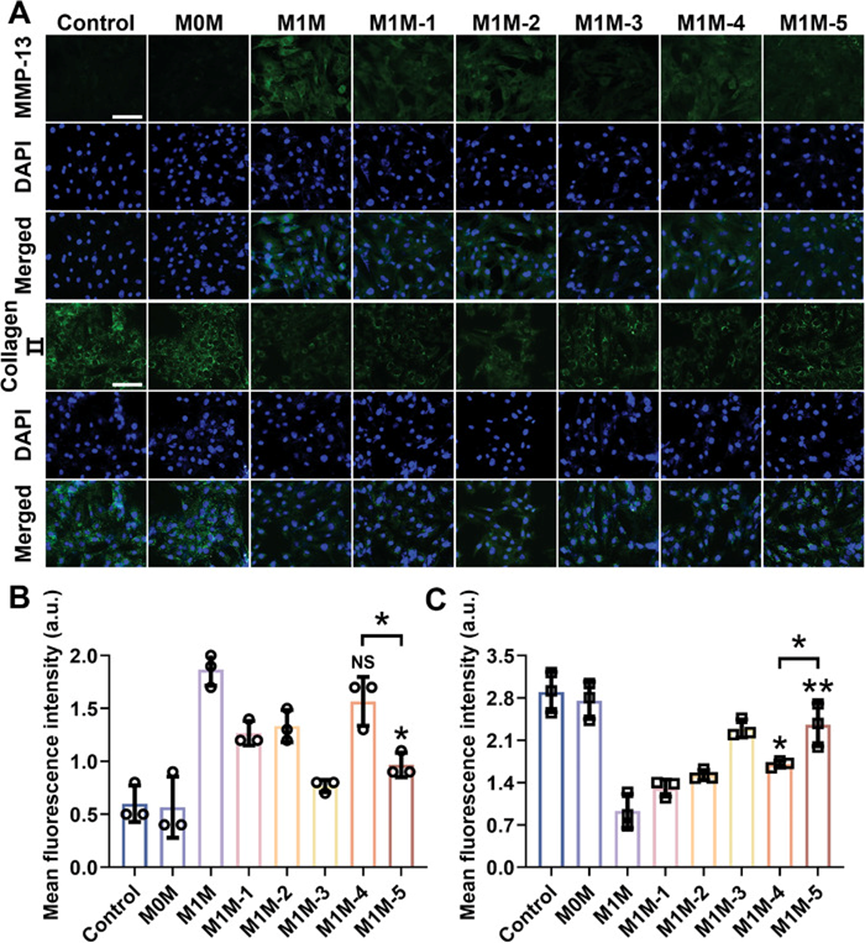
- 为了评估 RCC 的代谢活性,使用基质金属蛋白酶 (MMP)-13 作为分解代谢的指标,以胶原蛋白 II 作为合成代谢的指标进行了 IF 测定。对照组和 M0M 组中 MMP-13 信号较弱,而胶原蛋白 II 信号较强,表明 RCC 处于健康状态 (图A )。
- 然而,在 M1M 环境中培养后,MMP-13 的荧光强度增加,胶原蛋白 II 的荧光强度显着降低,表明 RCC 中的代谢稳态被打破,软骨细胞转变为类似 OA 的病理状态。相反,与其他治疗组相比,M1M-5 组的 MMP-13 荧光显著降低,而胶原蛋白 II 荧光强度显著增加。
- 定量荧光分析证实了这些结果(图B、C)。IF 测定表明 IgG/BRJ 可有效抑制分解代谢酶的表达并保护 RCC。
IgG/BRJ 促进巨噬细胞 M1 向 M2 极化
A) 在不同条件培养基中培养的 RCC 的 MMP-13 和胶原蛋白 II IF 图像。比例尺 = 100 µm。
B) MMP-13 荧光强度的定量分析。
C) 胶原蛋白 II 荧光强度的定量分析。

动物体内实验论证 IgG/BRJ对OA的体内治疗效果及潜在机制
一、体内活体成像:
为了测试 IgG/BRJ 的体内治疗效果,使用近红外染料 1,1′-双十八烷基-3,3,3′,3′-四甲基吲哚三羰菁碘化物 (DiR) 评估了纳米颗粒在关节内注射后的滞留情况,以追踪不同的制剂,包括游离 DiR、DiR@BRJ 和 IgG/DiR@BRJ,并使用体内成像系统 (IVIS)。
- 构建OA动物模型
- 比较了纳米颗粒在 OA (图 A ) 和健康关节 (图 B ) 中的体内行为。结果表明,在健康和 OA 关节中,关节内注射 24 小时后,游离 DiR 的信号均显着下降。这种快速的信号下降与以前的报道一致,因为小分子通常通过淋巴管或毛细血管迅速排泄。
- 相比之下,DiR@BRJ 和 IgG/DiR@BRJ 组在关节内注射 24 至 168 小时后表现出比游离 DiR 更好的保留性。
- 有趣的是,在 24 到 120 小时内,OA 关节中的荧光信号比健康关节中的衰减更快(图 C)。这种差异归因于 OA 环境中 ROS 水平的升高,这加速了纳米颗粒药物的释放。
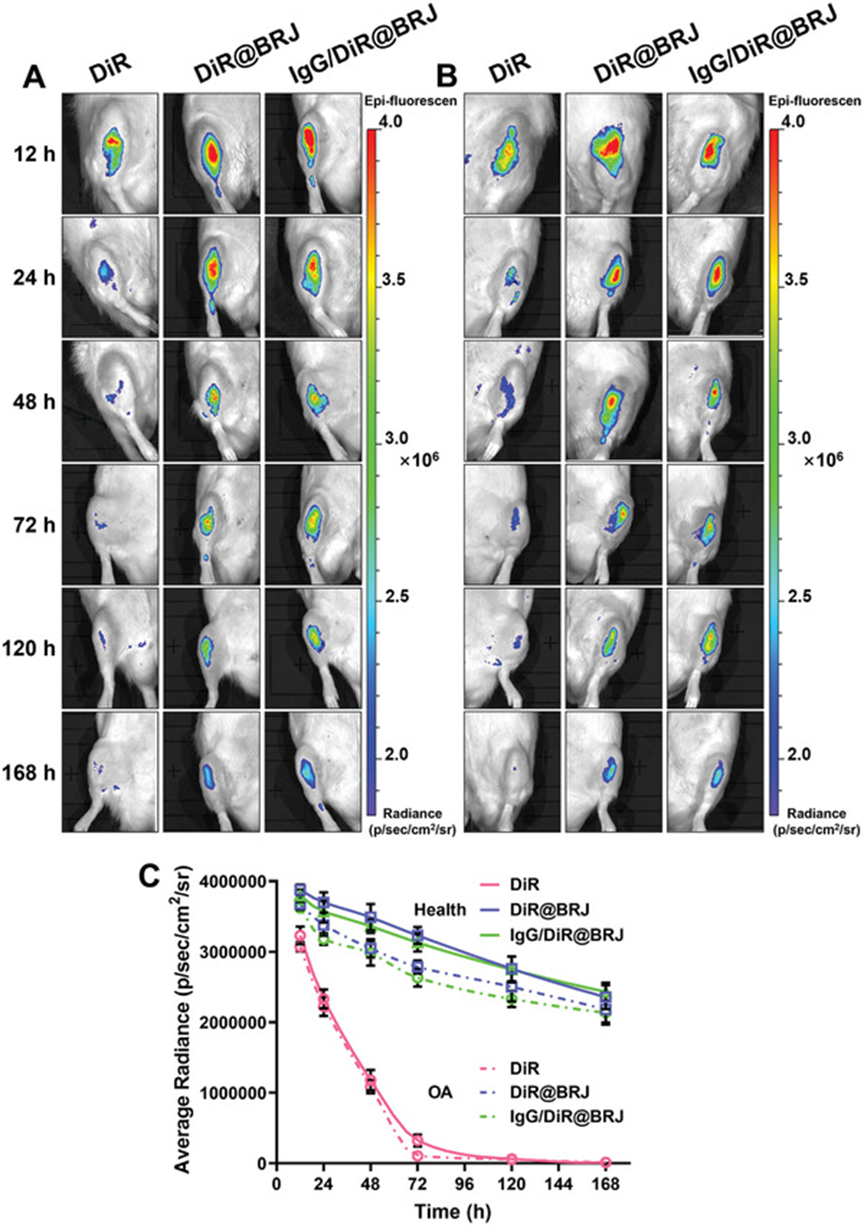
将IgG/DiR@BRJ注射到健康或OA大鼠膝关节后进行体内成像
在注射后12、24、48、72、120和168小时,通过DiR追踪纳米粒子在体内的全过程。
A) OA膝关节。
B) 健康膝关节。
C) 不同时间段健康或OA膝关节荧光强度的定量分析。
二、Micro-CT扫描分析:
为了进行后续的体内评估,使用前交叉韧带横断 (ACLT) 大鼠来评估 IgG/BRJ 的治疗效果。术后第 35 天,将大鼠随机分为 6 组,以假手术大鼠作为健康对照。
- ACLT 组每 5 天在右膝关节内注射生理盐水、BR+J、BRJ、IgG/BRJ 和透明质酸 (HA)。从临床角度来看,HA 被用作阳性对照。
- 在第 65 天,对大鼠实施安乐死,并收集其关节用于进一步实验(图A)。与假手术组相比,ACLT 组关节肿胀严重。
- 然而,药物治疗组的关节肿胀得到一定程度的改善。关节解剖暴露关节腔后,ACLT组软骨出现严重缺损。
- 相比之下,IgG/BRJ治疗组软骨缺损明显改善,软骨表面明显更光滑,与假手术组相似。其他治疗组虽然也表现出一定疗效,但在维护软骨完整性方面不如IgG/BRJ。
- 为了进一步评估ACLT后膝关节骨赘及软骨下骨损伤情况,进行了微型计算机断层扫描(Micro-CT)。膝关节二维矢状面和冠状面扫描图像显示骨赘以黄色箭头标出(图B)。在ACLT组中,Micro-CT图像显示骨赘形成明显增多,表面出现严重的凹坑和裂纹,提示软骨和软骨下骨损伤严重。
- 相反,IgG/BRJ治疗组疗效最佳,骨赘形成最少,软骨下骨完整。通过量化总骨赘体积(图C)和宏观评分(图 D)进一步证实了这一观察结果,表明IgG/BRJ可有效保护软骨并延缓OA进展。
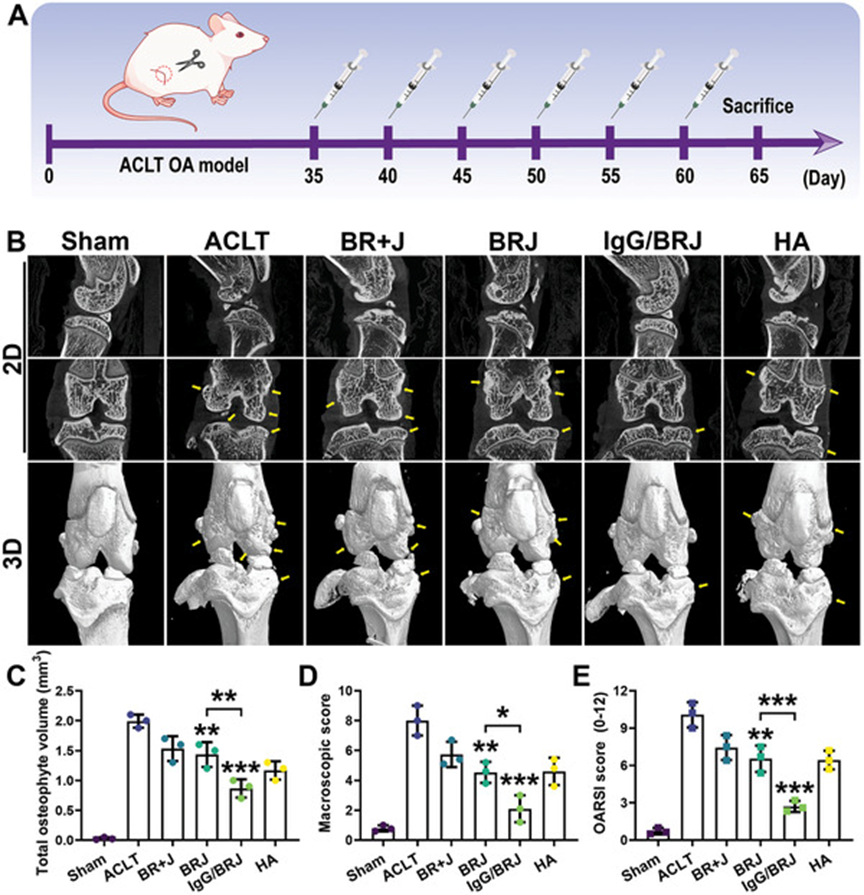
IgG/BRJ 在骨关节炎 (OA) 模型中的体内治疗效果
A) 体内实验设计。
B) 大鼠膝关节的二维和三维宏观 CT 图像(黄色箭头指示骨赘)。
C) 大鼠膝关节骨赘总体积的量化。
D) 软骨宏观评分。
E) 软骨 OARIS 评分。
三、骨组织染色及免疫组化:
进一步采用苏木精-伊红 (H&E) 染色、番红 O 和固绿染色以及甲苯胺蓝染色对软骨组织进行组织学评估,评估治疗后 OA 的软骨状况。
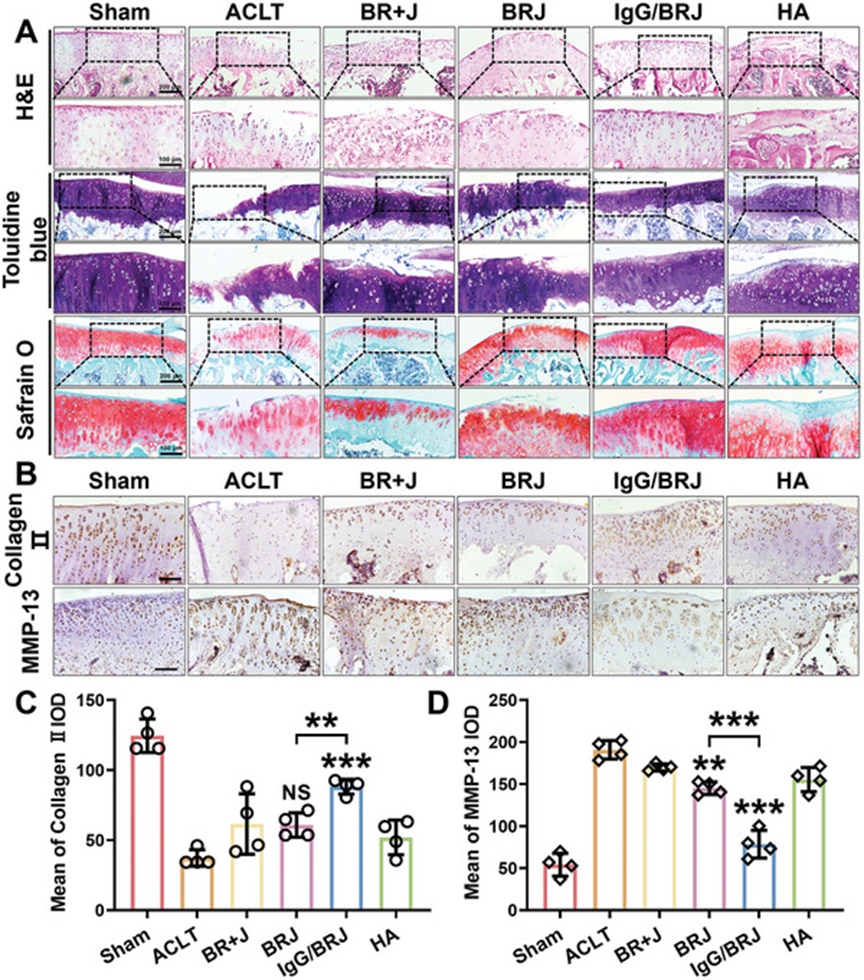
- ACLT 组软骨破坏最为严重,表现为表面不平整、细胞变性和 ECM 降解(图A)。相比之下,假手术组软骨表面光滑。
- 值得注意的是,严重损伤的软骨在 IgG/BRJ 治疗后变得更光滑,结构更完整,表明其具有潜在的软骨修复能力。
- 番红O-固绿和甲苯胺蓝染色进一步证实了 ACLT 组软骨损伤程度,其中糖胺聚糖 (GAG) 分布不均且明显减少。在各治疗组(BR+J、BRJ、HA)中,软骨损伤均有不同程度的减轻,其中IgG/BRJ组的GAG含量最高,与假手术组相当。
- 为了评估软骨的代谢活性,进行了免疫组织化学 (IHC) 检测,以测量胶原蛋白 II 和 MMP-13 的水平。假手术组 MMP-13 水平较低,胶原蛋白 II 水平较高,提示代谢状态健康(图B-D)。相反,ACLT 组 MMP-13 表达升高,胶原蛋白 II 表达降低,提示软骨以分解代谢为主。然而,经 IgG/BRJ 治疗后,软骨中 MMP-13 的高表达降低,而胶原蛋白 II 水平显著升高,提示软骨的代谢活性转向更正常的状态。
IgG/BRJ 对软骨修复的影响
A) 经 H&E、甲苯胺蓝和番红 O 染色的膝关节软骨切片。
B) 膝关节软骨中胶原蛋白 II 和 MMP-13 的免疫组织化学 (IHC) 检测。比例尺 = 100 µm。
C、D) (B) 的定量分析。
四、滑膜组织染色、免疫组化及免疫荧光
滑膜炎与 OA 的进展和发病机制之间的复杂关联最近已被证实;因此,对滑膜进行了组织学评估。
- H&E 染色显示,ACLT 组的滑膜结构严重破坏和增厚,炎症细胞浸润明显(图A)。
- 然而,IgG/BRJ 治疗通过促进滑膜组织网状结构的修复和抑制炎症细胞浸润改善了这种影响。为了进一步评估滑膜的炎症状态,进行了 IHC 检测以评估 TNF‐α 的表达。ACLT 组的 TNF‐α 表达显著上调(图B、D)。
- 然而,在施用不同制剂后,这种上调在不同程度上被逆转,其中 IgG/BRJ 治疗组的抑制最为明显。 H&E染色和IHC结果显示IgG/BRJ能明显抑制滑膜炎症。
- 为了探讨IgG/BRJ对巨噬细胞表型的调节作用,采用IF实验,以CD86(M1型生物标志物)和Arg-1(M2型生物标志物)两种指标,分析OA滑膜浸润的巨噬细胞类型(图10C)。定量分析(图 E、F)显示,ACLT组CD86的荧光信号强度明显增加,提示M1型巨噬细胞占主导地位,而Arg-1的荧光信号强度与假手术组无明显差异,提示M2型巨噬细胞的存在有限。然而,经过IgG/BRJ治疗后,CD86的荧光信号强度明显降低,而Arg-1的荧光信号强度明显增加。这些结果表明,IgG/BRJ 的给药可促进 OA 滑膜中 M1 巨噬细胞转化为 M2 巨噬细胞。
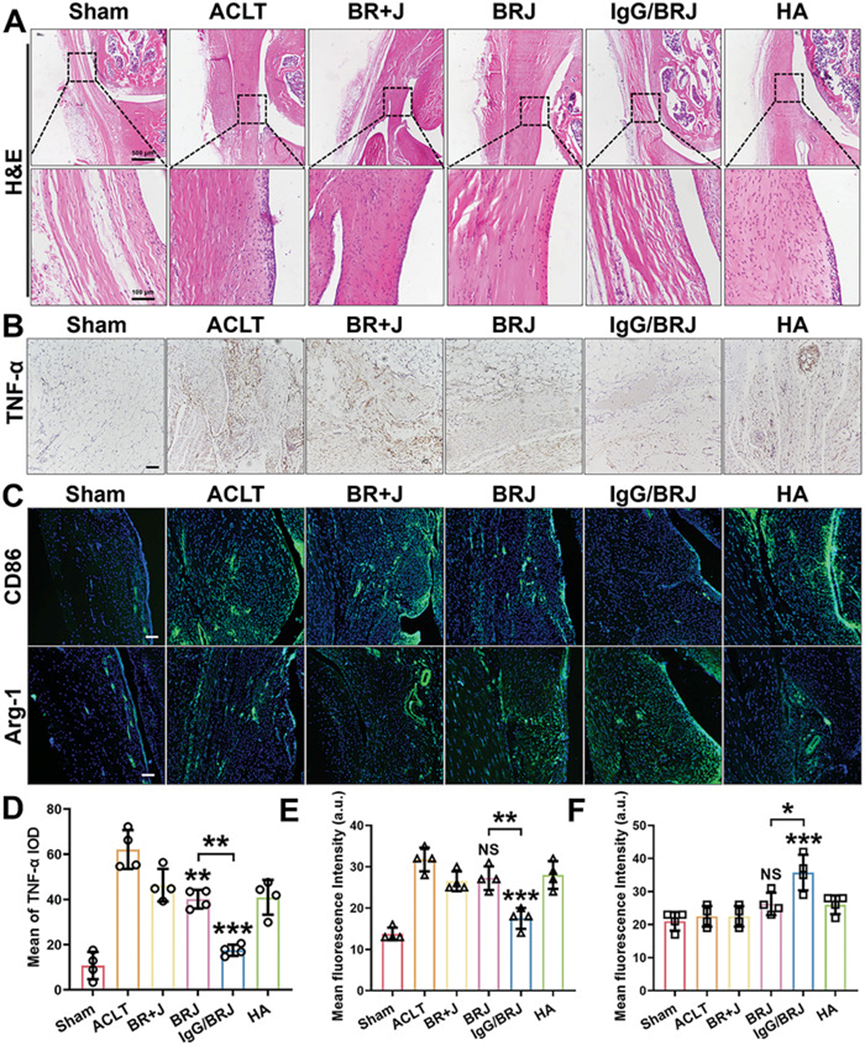
不同治疗后滑膜的组织学分析
A) 滑膜的 H&E 染色。黑框放大了滑膜区域的炎症细胞。
B) 不同治疗后滑膜的 IHC 检测。比例尺 = 100 µm。
C) 滑膜中 CD86 和 Arg-1 的 IF 检测。比例尺 = 100 µm。
D) (B) 的定量分析。
E,F) (C) 中荧光强度的定量分析。

结论
IgG/BRJ 干预可通过调节 M1-M2 巨噬细胞极化来促进软骨修复和再生,使其成为治疗骨关节炎 (OA) 的有效且有前景的选择。组织学和免疫组织化学证据进一步支持了 IgG/BRJ 作为缓解 OA 相关病理改变和促进软骨修复的治疗候选药物的潜力。
